Apixaban bewährt sich bei Krebspatient:innen mit VTE auch im Versorgungsalltag
In der CARAVAGGIO-Studie zeigte Apixaban (ELIQUIS<sup>®</sup>) ein gutes Wirksamkeits- und Sicherheitsprofil bei der Behandlung und Rezidivprophylaxe krebsassoziierter venöser Thromboembolien (VTE) – auch bezüglich gastrointestinaler (GI-)Blutungen. Aber lassen sich diese Daten auch in den klinischen Alltag übertragen?
Im klinischen Alltag müssen nicht selten komplexe Situationen gelöst werden – z. B. bleibt die Antikoagulation bei krebsassoziierten venösen Thromboembolien eine Herausforderung:
VTE sind die zweithäufigste Todesursache bei Patient:innen mit einer Tumorerkrankung.1 Auch unter Antikoagulation ist das Risiko für VTE bzw. VTE-Rezidive sowie für schwere Blutungen bei Krebspatient:innen höher als bei Patient:innen ohne Tumorerkrankung.2
Alleinige Standardtherapie für diese Risikosituation waren viele Jahre die subkutan zu injizierenden, niedermolekularen Heparine (NMH). Dabei wäre gerade bei Krebspatient:innen in vielen Fällen psychologisch eine ambulante orale Behandlung wünschenswert.
Krebsassoziierte VTE wirksam oral behandeln – ohne Abstriche in bei der Verträglichkeit
Der Faktor-Xa-Hemmer Apixaban war in der randomisierten klinischen Studie (RCT) CARAVAGGIO3 dem niedermolekularen Heparin (NMH) Dalteparin bei der Verhinderung von VTE-Rezidiven nicht unterlegen, ohne mit einem Anstieg des Risikos für schwere Blutungen* assoziiert zu sein.3 Dies galt auch für die gefürchteten gastrointestinalen (GI-)Blutungen (siehe Akkordeon oder diese Infografik).3
Nun liegen für Apixaban auch aktuelle Daten zur Behandlung krebsassoziierter VTE aus dem US-amerikanischen Versorgungsalltag4,+, vor. Zeigte die Behandlung mit Apixaban unter Alltagsbedingungen ähnliche Ergebnisse wie die klinische Studie?
Daten von 14.086 Erwachsenen aus dem Versorgungsalltag
Für ihre retrospektive Analyse untersuchten Cohen et al. die Daten aus vier US-amerikanischen Versicherungsdatenbanken über den Zeitraum von März 2014 an über bis zu vier Jahre. Eingeschlossen wurden insgesamt 14.086 erwachsene Patient:innen mit aktiver Krebserkrankung und mindestens einer Neuverschreibung für eine VTE-Behandlung mit Apixaban (n = 3.393), NMH (n = 6.108) oder dem Vitamin-K-Antagonisten Warfarin (n = 4.585) innerhalb von 30 Tagen nach der VTE-Diagnose. Im Weiteren liegt unser Fokus auf dem Vergleich Apixaban versus NMH, da NMH bislang die leitliniengerechte Standardtherapie für krebsassoziierte VTE war.4
Mehr zur Studienpopulation
Als Index-Ereignis berücksichtigt wurden VTE-Diagnosen mit ≥ 1 Verordnung für VTE-Behandlung in der Klinik oder ambulant zwischen dem 1. März 2014 und dem Studienende (Market Scan: 30. Juni 2017; Humana und Optum: 31. Dezember 2017; PharmMetrics: 31. März 2018). Etwa 42 % der Patient:innen hatten als Einschlussdiagnose eine LE mit/ohne TVT, ca. 58 % nur eine TVT.4
Aus dieser Population wurden Krebspatient:innen ermittelt über mind. zwei Krankenversicherungsansprüche für eine Krebsdiagnose oder einen Krankenversicherungsanspruch für eine Krebsdiagnose und mind. eine Verschreibung für eine Krebsbehandlung sechs Monate vor oder 30 Tage nach VTE-Ereignis.4
Die Ausgewogenheit der Patient:innencharakteristika wurde über die IPT-Gewichtung (inverse probability treatment weighting, IPTW) gewährleistet.4
Wichtige Ausschlusskriterien waren nicht-melanozytärer Hautkrebs sowie eine Antikoagulation oder VTE-Diagnose innerhalb von sechs Monaten vor dem Index-VTE-Ereignis.4
Die Ergebnisse Apixaban versus Standard- NMH im Einzelnen
Die Antikoagulation mit Apixaban war nach sechs Monaten im Vergleich zu NMH assoziiert mit (siehe Abb. 1):
- weniger VTE-Rezidiven‡ (Effektivitätsendpunkt; Hazard Ratio [HR] = 0,61; 95 %-Konfidenzintervall [KI]: 0,47–0,81; p = 0,001)4
- weniger schweren Blutungen‡ (Verträglichkeitsendpunkt; HR = 0,63; 95 %-KI: 0,47–0,86; p = 0,003)4
- vergleichbaren Raten an schweren GI-Blutungen (HR = 0,97; 95 %-KI: 0,59–1,58; p = 0,892).4
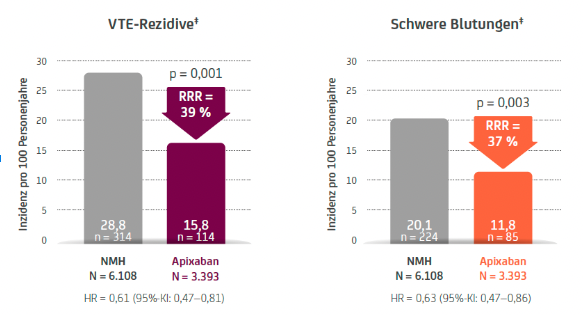
Abb. 1: Ergebnisse zum Effektivitätsendpunkt „VTE-Rezidive“ und dem Verträglichkeitsendpunkt „schwere Blutungen“ unter Apixaban versus NMH aus dem US-Versorgungsalltag. Grafik adaptiert nach Cohen et al. 2021.4
Antikoagulation bei GI-Tumor und Krebsbehandlung
In einer weiteren Subgruppenanalyse richteten Cohen et al. besonderes Augenmerk auf zwei relevante Hochrisikogruppen:
- Bei Patient:innen mit GI-Tumor waren relevante Ergebnisse konsistent zur Hauptanalyse der CARAVAGGIO-Studie. Dies galt unter anderem für den Wirksamkeitsendpunkt VTE-Rezidive‡ (HR = 0,94; 95 %-KI: 0,48-1,82), den Sicherheitsendpunkt schwere Blutungen‡ (HR = 0,74; 95 %-KI: 0,38-1,42) sowie für schwere GI-Blutungen (HR = 1,07; 95 %-KI: 0,46-2,49).5
- Bei Patient:innen mit Krebsbehandlung/Chemotherapie$ wurde ebenfalls ein zur Hauptanalyse konsistentes Nutzen/Risiko-Profil beobachtet.5
Unterschiede in der Therapietreue nach 6 Monaten
In der Analyse aus dem US-Versorgungsalltag wurden außerdem Angaben zur Therapietreue gemacht: Während fast zwei von drei Patient:innen (61,0 %), die NMH erhielten, die Therapie wechselten oder abbrachen, war es bei Apixaban nur etwas mehr als eine:r von drei Patient:innen (39,4 %).4
CHEST-Guideline: Faktor-Xa-Hemmer erste Option bei krebsassoziierter VTE
Die Daten aus dem US-Versorgungsalltag ergänzen das gute Wirksamkeits- und Sicherheitsprofil von Apixaban bei der Behandlung krebsassoziierter VTE aus der RCT-Studie CARAVAGGIO3 ‒ auch bei Hochrisiko-Patient:innen mit gleichzeitiger Krebsbehandlung/Chemotherapie oder mit GI-Tumoren.4, 5
Wichtig für die Praxis ist die Umsetzung der aktuellen CHEST-Guidelines.6 Diese empfehlen orale Faktor Xa-Inhibitoren inzwischen vor NMH für die Behandlung einer akuten tumorassoziierter VTE, differenzieren aber bei der Behandlung von Patient:innen mit GI-Tumoren: Für diese können Apixaban oder NMH die bevorzugte Option sein.6
Die multinationale, prospektive, randomisierte, offene Studie mit verblindeter Endpunktauswertung (PROBE-Design) evaluierte über sechs Monate 1:1 randomisiert die Wirksamkeit und Sicherheit von
-
Apixaban (10 mg 2 x täglich bis Tag 7, gefolgt von 5 mg 2 x täglich); n = 576
- versus Dalteparin (200 I.E./kg Körpergewicht [KG] 1 x täglich bis Tag 30, dann 150 I.E./kg KG 1 x täglich); n = 579
bei 1.170 erwachsenen Krebspatient:innen mit neu diagnostizierter, proximaler tiefer Venenthrombose (TVT) der unteren Extremität und/oder Lungenembolie (LE).3
Behandelt wurde über 6 Monate mit einer anschließenden Nachbeobachtungszeit von 30 Tagen.3
Ergebnisse
- Primärer Wirksamkeitsendpunkt VTE-Rezidive: Zu VTE-Rezidiven kam es unter Apixaban bei 5,6 % der Patient:innen versus 7,9 % unter Dalteparin (HR 0,63; 95 %-KI: 0,37-1,07; p < 0,001 für Nicht-Unterlegenheit und p = 0,09 für Überlegenheit).
- Haupt-Sicherheitsendpunkt schwere Blutungen*: Die Rate schwerer Blutungen mit 3,8 % (Apixaban) versus 4,0 % (Dalteparin) vergleichbar (HR 0,82; 95 %-KI 0,40–1,69; p=0,60).
-
Schwere gastrointestinale Blutungen: Es zeigte sich kein signifikanter Unterschied (1,9 % versus 1,7 %; HR = 1,05; 95 %-KI: 0,44-2,50).
Im sekundären Endpunkt Ereignisfreies Überleben (Nichtauftreten von VTE-Rezidiven, schweren Blutungen oder Tod) war Apixaban mit 73,3 % versus 68,6 % überlegen (HR = 1,36; 95 %-KI: 1,05-1,76). Subgruppenanalysen der CARAVAGGIO-Studie zeigten zudem, dass eine gleichzeitige Krebsbehandlung keinen offensichtlichen Effekt auf die Raten an VTE-Rezidiven oder schweren Blutungen* unter Apixaban oder Dalteparin hatte.7 Unabhängig von der Tumorlokalisation waren die Raten an schweren Blutungen in beiden Behandlungsarmen vergleichbar.8
* EMA-Definition: schwere Blutungen nach Kriterien der International Society on Thrombosis and Haemostasis (ISTH) oder Blutungen, die einen akuten chirurgischen Eingriff erfordern.
* Definition: schwere Blutungen nach Kriterien der International Society on Thrombosis and Haemostasis (ISTH) oder Blutungen, die einen akuten chirurgischen Eingriff erfordern.
+ Limitationen:• Beobachtungsstudien zeigen nur Assoziationen zwischen Variablen, keine Kausalität.• Die Definitionen von VTE-Rezidiven basierte auf der stationären Diagnose nach ICD-9/10-CM für VTE mit positiver Risikoabschätzung (26–93 %). Patient:innen mit anderen Hospitalisierungsgründen und VTE wurden dadurch nicht ausgeschlossen.• Hämoglobinwerte waren nicht verfügbar, daher ist es theoretisch möglich, dass nicht alle schweren Blutungen erfasst wurden. • Die ICD-Codes und der Algorithmus zur Identifikation von CRNM Blutungen sind nicht in der Literatur validiert. Eine Fehleinschätzung aufgrund falscher Klassifizierung ist möglich. • Das Poolen der Datensätze ermöglicht keinen Ausschluss von Duplikaten. Schätzungen in der Literatur gehen von nur 0,5 % Duplikaten aus.• Wie bei jeder Versicherungsdatenbank besteht die Möglichkeit von Kodierungsfehlern und fehlenden Daten.• Es wurden 52 Patient:innen mit VTE-Rezidiven während der Überbrückungsphase mit NMH vor Warfarin ausgeschlossen.• Kommerzielle Datenbanken enthalten keine Informationen zu Todesfällen wie fatalen VTE-Rezidiven.• Die Ergebnisse treffen unter Umständen nur auf die erfasste Population (privat krankenversicherte US-Amerikaner:innen) zu.• Bestimmte Daten wie z. B. Laborparameter sind bei den Versicherungsdaten nicht verfügbar.• In den Datensätzen sind Verschreibungen von Medikamenten während der Hospitalisierung nicht identifizierbar.
‡ VTE-Rezidive und schwere Blutungen wurden identifiziert anhand der ersten angegebenen Diagnose einer VTE oder schweren Blutung im Krankenhaus. Zur Codierung wurde u.a. ICD-9-CM, ICD-10-CM verwendet. Hospitalisierungen mit VTE-Diagnose, die innerhalb von 7 Tagen nach der Index-VTE erfolgten, wurden nicht als VTE-Rezidiv gewertet. Schwere Blutungen beinhalteten GI-, intrakranielle und schwere Blutungen an anderen Stellen.
$ 6 Monate vor bis 30 Tage nach Index- Datum.
- Khorana AA et al. J Thromb Haemost. 2007; 5(3):632–634. doi:10.1111/j.1538-7836.2007.02374.x
- Prandoni P et al. Blood. 2002; 100(10):3484–3488. doi:10.1182/blood-2002-01-0108
- Agnelli G et al. N Engl J Med. 2020; Apr 23;382(17):1599-1607. doi:10.1056/NEJMoa1915103
- Cohen A et al. Thromb Haemost. 2021; 121(3):383–395. doi:10.1055/s-0040-1718728
- Cohen AT et al. Curr Med Res Opin. 2021:1–16. doi:10.1080/03007995.2021.1932448
- Stevens SM et al. Chest. 2021. doi:10.1016/j.chest.2021.07.056
- Verso M et al. Eur J Cancer. 2021; 148:371–381. doi:10.1016/j.ejca.2021.02.026
- Ageno W et al. Thromb Haemost. 2021; 121(05):616–624. doi:10.1055/s-0040-1720975
