- Hindricks G und Potpara T et al. Eur Heart J. 2021;42(5):373–498.
- Schäfer A, et al. Cardiovasc Drugs Ther. 2020;34(4):555–68.
- Granger CB, et al. N Engl J Med. 2011;365(11):981–92.
- Connolly SJ, et al. N Engl J Med. 2009;361(12):1139–51.
- Patel MR, et al. N Engl J Med. 2011;365(10):883–91.
- Giugliano RP, et al. N Engl J Med. 2013;369(22):2093–104.
NOACs: mehr Wirksamkeit, mehr Blutungsrisiko?
Wenn Sie an Ihre ≥ 75 jährigen Patient:innen mit nicht-valvulärem Vorhofflimmern (VHF<sup>♦</sup>) denken, wägen Sie dann im Geiste ab, ob die geringere Rate an thromboembolischen Ereignissen bei NOACs – verglichen mit VKA – ein höheres Risiko für schwere Blutungen birgt? Eine Subanalyse von Daten aus den NOAC-Zulassungsstudien mit Fokus auf VHF<sup>♦</sup>-Patient:innen ab 75 Jahren gibt Antworten.
Diese Konstellation dürfte auch in Ihrer Praxis nicht selten sein: Eine 79-jährige Patientin mit VHF♦︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎, Herzinsuffizienz und Hypertonie, möglicherweise auch einer moderaten Nierenfunktionseinschränkung. Schon aufgrund ihres Alters von ≥ 75 Jahren ist für die Patientin eine orale Antikoagulation (OAC) zur Prophylaxe von Schlaganfällen und systemischen Embolien angezeigt.1 Wird eine OAC bei VHF♦︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎-Patient:innen begonnen, für die sich ein NOAC eignet, wird laut ESC Leitlinie ein NOAC bevorzugt vor VKA empfohlen.1
Gerade für VHF♦︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎-Patient:innen ≥ 75 Jahre ist eine Nutzen-Risiko-Bewertung für eine Antikoagulation von besonderer Bedeutung: aufgrund ihres Alters und dem damit verbundenen gesteigerten Risiko für Thromboembolien und schwere Blutungen, aber auch aufgrund von Komorbiditäten und Komedikationen. Um die Wirksamkeit und Sicherheit der NOACs bei VHF♦︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎-Patient:innen ≥ 75 Jahre gezielt zu untersuchen, analysierten Schäfer et al.2 die Daten aus den NOAC-Zulassungsstudien (ARISTOTLE n = 5.678 )3, (RE-LY n = 7.528)4, (ROCKET-AF n = 6.229)5 und (ENGAGE-AF n = 5.668)6.
Ein direkter Vergleich zwischen den einzelnen NOACs ist wegen Unterschieden der Studien in Design, Population und Definition für schwere Blutungen nicht möglich – die Daten können aber einen wichtigen Beitrag zur klinischen Nettonutzenabschätzung der NOACs verglichen mit VKA wie Warfarin leisten.
Klinischer Nettonutzen für Apixaban vs. Warfarin gezeigt
Alle vier NOACs verhinderten bei VHF♦︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎-Patient:innen ≥ 75 Jahre Schlaganfälle oder systemische Embolien mindestens so wirksam wie Warfarin (siehe Abschnitt "Ergebnisse zur Wirksamkeit und Sicherheit in Kürze"). Aber ist das mit einer erhöhten Blutungsrate verbunden?
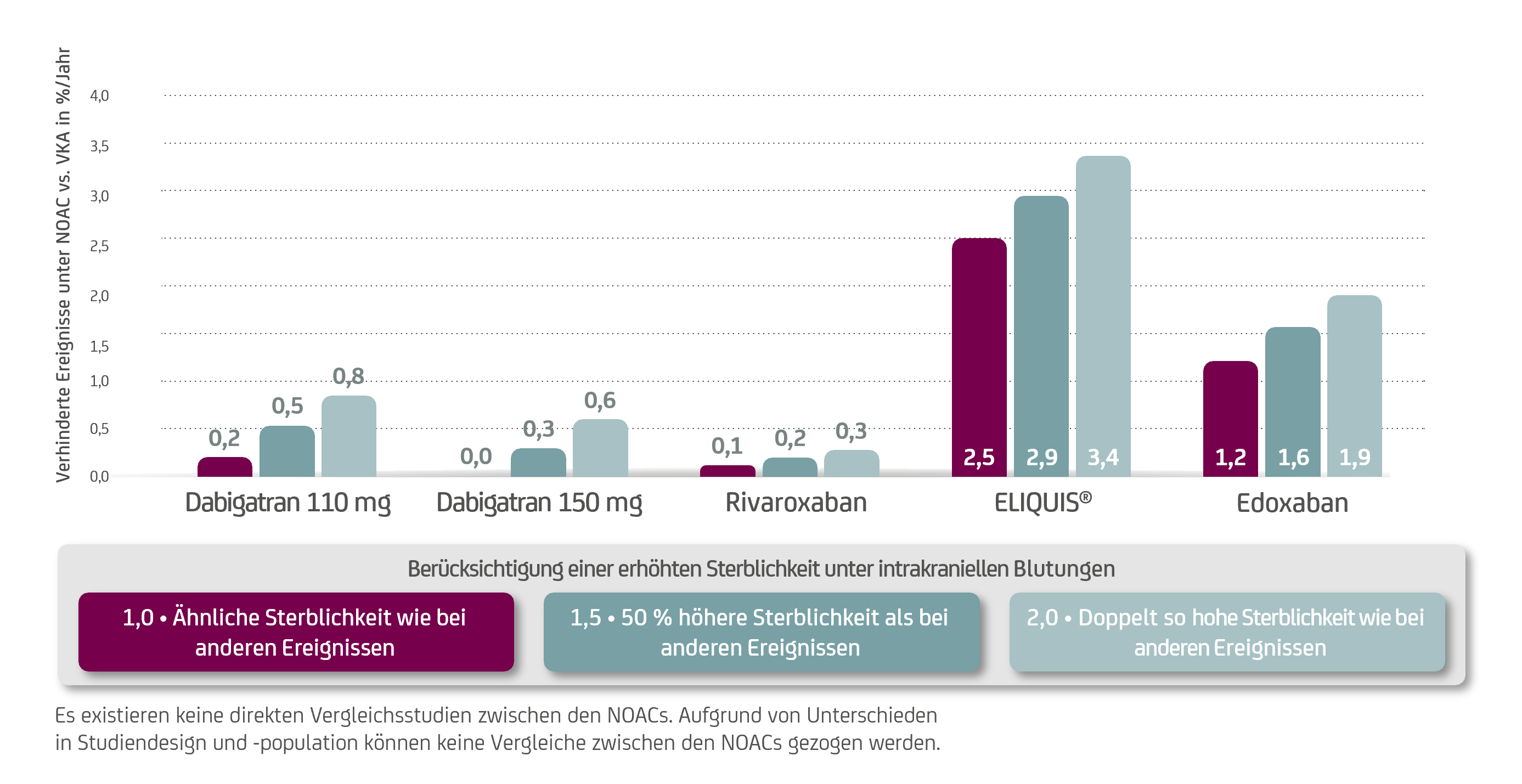
Die Analyse von Schäfer et al.2 zum klinischen Nettonutzen legt nahe, dass beim Einsatz von NOAC statt VKA bei VHF♦︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎-Patient:innen ≥ 75 Jahre weniger Schlaganfälle nicht automatisch mit vermehrten schweren Blutungen einhergehen. Der klinische Nettonutzen errechnet sich durch die jährliche Rate verhinderter thromboembolischer Ereignisse abzüglich der jährlichen Rate verursachter schwerer Blutungen (intrakranielle* plus andere schwere Blutungen). In der Auswertung war Apixaban mit dem größten klinischen Nettonutzen gegenüber Warfarin assoziiert, vor Edoxaban, Dabigatran und Rivaroxaban (Abb. 2).2
Abbildung 2: Klinischer Nutzen der einzelnen NOACs versus VKA bei Patient:innen ≥ 75 Jahre; adaptiert nach Schäfer et al.2
GI-Blutungen unter Apixaban vs. VKA vergleichbar
Gastrointestinale (GI-) Blutungen gehören wie auch intrakranielle Blutungen zu den schwerwiegendsten Komplikationen unter einer Antikoagulation. Analog zur Gesamtpopulation der ARISTOTLE-Studie3 zeigten sich für Apixaban bei der Analyse der VHF♦︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎-Patient:innen ≥ 75 Jahre vergleichbare Raten für schwere GI-Blutungen wie unter Warfarin (Hazard Ratio [HR] 0,99; 95 %-Konfidenzintervall [KI]: 0,69-1,42).2
Bei den anderen NOACs traten schwere GI-Blutungen verglichen mit Warfarin dagegen tendenziell häufiger auf (HR 1,69; 95 %-KI: 1,19-2,39 für Rivaroxaban; HR 1,39; 95 %-KI: 1,03-1,98 für Dabigatran 110 mg bzw. HR 1,79; 95 %-KI:1,35-2,37 für Dabigatran 150 mg; HR 1,32; 95 %-KI: 1,01-1,72 für Edoxaban).2
Ergebnisse zur Wirksamkeit und Sicherheit in Kürze
In der Analyse von Schäfer et al. waren bei VHF♦︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎-Patient:innen ≥ 75 Jahre die Raten an Schlaganfällen oder systemischen Embolien für Apixaban und Dabigatran 150 mg gegenüber Warfarin geringer bzw. im Fall von Rivaroxaban, Edoxaban, Dabigatran 110 mg vergleichbar – bei Blutungsraten, die für Apixaban† und Edoxaban† geringer waren als unter Warfarin und für Rivaroxaban‡, Dabigatran 110 mg 2 x tgl.§ und Dabigatran 150 mg 2 x tgl.§ vergleichbar mit Warfarin. 2
Fazit: Bei VHF♦︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎-Patient:innen ≥ 75 Jahre zeigte Apixaban im Vergleich zu Warfarin vor den anderen NOACs den höchsten klinischen Nettonutzen. Dabei ist auch das gegenüber Warfarin vergleichbare Risiko für schwere GI-Blutungen von großer praktischer Relevanz.2
Sie möchten mehr zu den primären Wirksamkeits- und Sicherheitsdaten der Analyse von Schäfer et al.2 bei VHF♦︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎-Patient:innen ≥ 75 Jahren erfahren? Hier geht’s zu den ausführlichen Ergebnissen.
VHF♦︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎= nicht-valvuläres Vorhofflimmern
*Intrakranielle Blutungen wurden mit einem Gewichtungsfaktor multipliziert. Der Gewichtungsfaktor berücksichtigt den relativen Einfluss, bezogen auf Tod und Behinderung, einer intrakraniellen Blutung unter OAC-Therapie gegenüber dem Auftreten eines ischämischen Schlaganfalls ohne Antikoagulation.
†Schwere Blutung definiert nach den Kriterien der International Society on Thrombosis and Haemostasis (ISTH): tödliche Blutung, Blutung in einem kritischen Bereich oder Organ (intrakranielle, intraspinale, intraokuläre, retroperitoneale, intraartikuläre, oder Perikardblutung oder intramuskuläre Blutung mit Kompartmentsyndrom), Blutung mit einem Hämoglobinabfall ≥ 2 g/dl, Transfusionsbedarf von ≥ 2 Einheiten Erythrozytenkonzentrat/Vollblut).
‡Schwere Blutung definiert als klinisch manifeste Blutung assoziiert mit tödlichem Ausgang, Beteiligung eines kritischen anatomischen Bereichs (intrakraniell, spinal, okular, perikardial, artikulär, retroperitoneal oder intramuskulär mit Kompartmentsyndrom), Hämoglobinabfall ≥ 2 g/dL, Transfusion mit ≥ 2 Einheiten Vollblut/Erythrozytenkonzentrat oder permanente Behinderung.
§Schwere Blutung definiert als Reduktion des Hämoglobin-Levels um mindestens 2 g/dL, Transfusion von mindestens 2 Einheiten Blut oder unter Erfordernis von inotropen Substanzen, symptomatische Blutungen in kritischem Bereich oder Organ.