- Schäfer A et al. Cardiovasc Drugs Ther. 2020; 34(4):555–568. doi:10.1007/s10557-020-06981-3
- Hindricks G und Potpara T et al. Eur Heart J. 2021; 42(5):373–498. doi:10.1093/eurheartj/ehaa612
- Granger CB et al. N Engl J Med. 2011; 365(11):981–992. doi:10.1056/NEJMoa1107039
- Connolly SJ et al. N Engl J Med. 2009; 361(12):1139–1151. doi:10.1056/NEJMoa0905561
- Patel MR et al. N Engl J Med. 2011; 365(10):883–891. doi:10.1056/NEJMoa1009638
- Giugliano RP et al. N Engl J Med. 2013; 369(22):2093–2104. doi:10.1056/NEJMoa1310907
Schlaganfallprophylaxe bei VHF<sup>♦</sup>: fürs Alter gewappnet?
Können Nicht-Vitamin-K-abhängige orale Antikoagulanzien (NOACs) bei ≥ 75 jährigen Patient:innen mit nicht-valvulärem Vorhofflimmern (VHF<sup>♦</sup>) einen vergleichbaren Schutz vor thromboembolischen Ereignissen bieten, wie in der allgemeinen Studienpopulation ‒ohne Zunahme schwerer Blutungen? Diese Frage hat eine Analyse der NOAC-Zulassungsstudien mit Fokus auf VHF<sup>♦</sup>-Patient:innen ab 75 Jahre untersucht.<sup>1</sup>
Bei VHF♦︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎-Patient:innen im Alter ≥ 75 Jahren ist, laut Leitlinie der European Society of Cardiology (ESC) für „Diagnose und Management von Vorhofflimmern“, allein aufgrund des Alters eine orale Antikoagulation (OAC) zur Prophylaxe von Schlaganfällen und systemischen Embolien empfohlen.2 Mit dem Alter steigt jedoch nicht nur das Schlaganfallrisiko, sondern auch das Risiko für Blutungsereignisse.2 Zudem können Begleiterkrankungen und deren medikamentöse Behandlung diese beiden Risiken nochmals erhöhen.2
Nutzen und Risiko einer Antikoagulation müssen bei VHF♦︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎-Patient:innen ≥ 75 Jahren also besonders abgewogen werden. Schäfer et al. analysierten daher die Daten von VHF♦︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎-Patient:innen ≥ 75 Jahren aus den vier NOAC-Zulassungsstudien, um die Wirksamkeit und Sicherheit der NOACs in dieser Risikopopulation zu untersuchen (ARISTOTLE3 n = 5.678, RE-LY4 n = 7.528, ROCKET-AF5 n = 6.229, ENGAGE-AF6 n = 5.668).1
Ein direkter Vergleich zwischen den einzelnen NOACs ist wegen Unterschieden der Studien in Design, Population und Definition für schwere Blutungen nicht möglich. Die Daten können aber einen wichtigen Beitrag zur Nutzen-Risiko-Abschätzung der NOACs zur Schlaganfallprophylaxe bei VHF♦︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎-Patient:innen, verglichen mit Vitamin-K-Antagonisten (VKA) wie Warfarin, leisten.
Apixaban bei VHF♦︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎-Patient:innen ≥ 75 Jahre: weniger thromboembolische Ereignisse bzw. schwere Blutungen vs. VKA
Für den Vergleich Apixaban versus Warfarin zeigte sich in den primären Wirksamkeits- und Sicherheitsendpunkten ein Bild, das konsistent zu den Ergebnissen der Gesamtpopulation der Zulassungsstudie war.1 Unter Apixaban reduzierten sich im Vergleich zu Warfarin sowohl die Raten an
- Schlaganfällen und systemischen Embolien (Hazard Ratio [HR] 0,71; 95 %-Konfidenzintervall [KI]: 0,53-0,95) als auch an
- schweren Blutungen* (HR 0,64; 95 %-KI: 0,52-0,79).1
Differenziertes Bild für verschiedene NOACs
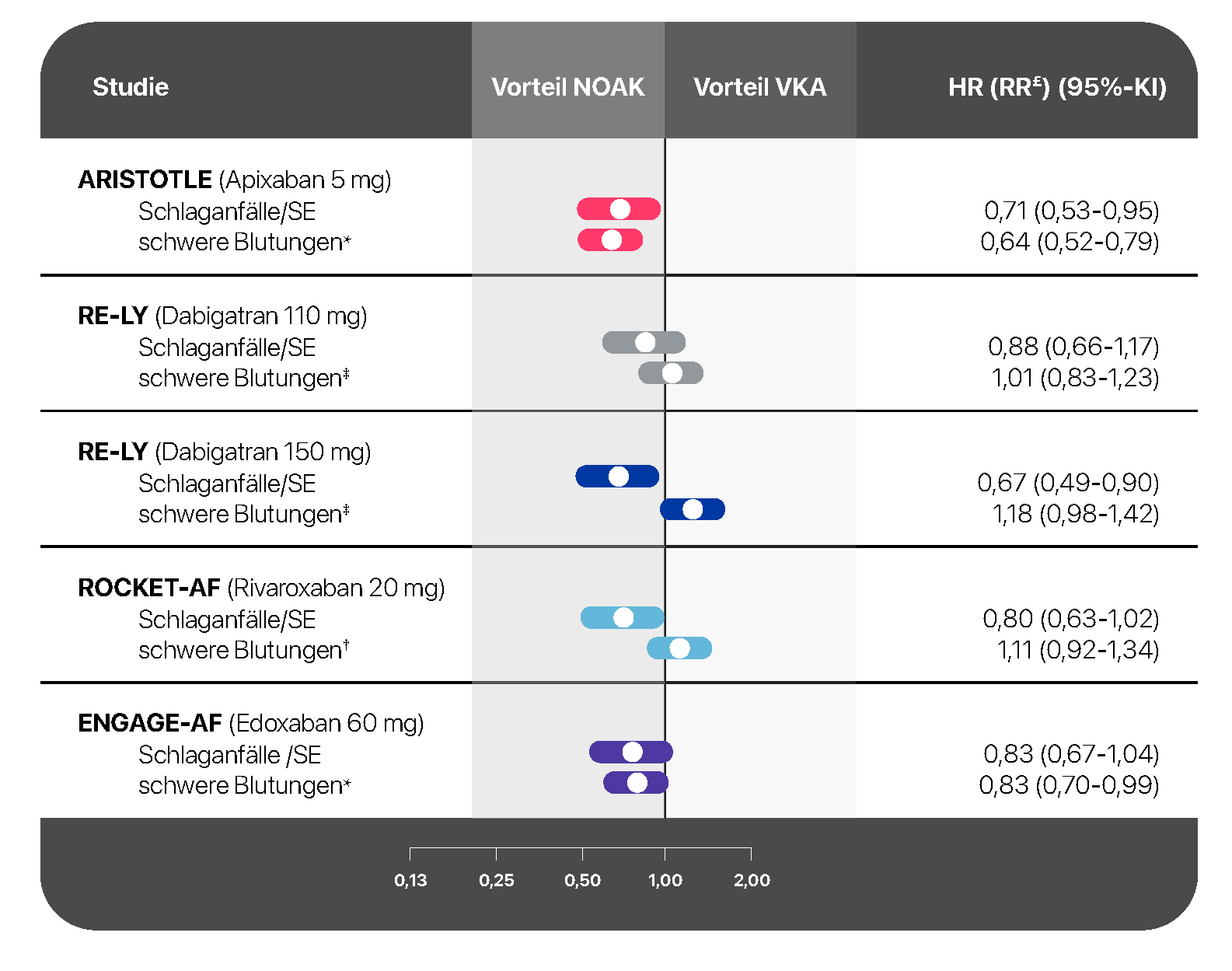
Während für Apixaban eine Reduktion beider Endpunkte auch bei VHF♦︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎-Patient:innen ≥ 75 Jahren beobachtet werden konnte, zeigten sich bei den anderen NOACs folgende Ergebnisse (Abb.1):
- Gegenüber Warfarin waren die Raten an Schlaganfällen oder systemischen Embolien vergleichbar bei Rivaroxaban (HR 0,80; 95 %-KI: 0,63‒1,02), Dabigatran 110 mg 2 x tgl. (Relative Risikoreduktion [RR] 0,88; 95 %-KI: 0,66‒1,17) sowie Edoxaban (HR 0,83; 95 %-KI: 0,67‒1,04) bzw. geringer für Dabigatran 150 mg 2 x tgl. (RR 0,67; 95 %-KI: 0,49‒0,90).
- Die Raten für schwere Blutungen waren vergleichbar mit Warfarin für Rivaroxaban† (HR 1,11; 95 %-KI: 0,92‒1,34), Dabigatran 110 mg 2 x tgl.‡ (RR 1,01; 95 %-KI: 0,83‒1,23) und Dabigatran 150 mg 2 x tgl.§ (RR 1,18; 95 %-KI: 0,98‒1,42) aber geringer unter Edoxaban* (HR 0,83; 95 %-KI: 0,70‒0,99).1
Damit stehen diese Ergebnisse für Apixaban, Rivaroxaban, Edoxaban und Dabigatran 150 mg 2 x tgl. im Einklang mit der Gesamtpopulation der jeweiligen Zulassungsstudie.3–6
Abb.: Daten zur Wirksamkeit und Sicherheit der einzelnen NOACs vs. Warfarin bei Patient:innen ≥ 75 Jahre, basierend auf Daten der Zulassungsstudien.3–6 Adaptiert nach Schäfer et al. 2020.1
Fazit: Apixaban zeigte beim Vergleich mit Warfarin für VHF♦︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎-Patient:innen ≥ 75 Jahren konsistente Daten zu den Ergebnissen der Hauptanalyse. Als einziges NOAC war Apixaban sowohl mit weniger Schlaganfällen oder systemischen Embolien als auch schweren Blutungen* assoziiert.1,3
Erleben Sie, wie Herr Prof. Schäfer die Ergebnisse seiner Analyse persönlich einordnet und schauen Sie sich unseren Webinar-Mitschnitt an. Nach Absolvieren des Wissenstests können Sie 2 CME-Punkte erhalten.
Schäfer et al. analysierten außerdem die Daten der Zulassungsstudien hinsichtlich auftretender Gastrointestinaler (GI)-Blutungen und des klinischen Nettonutzens der NOACs bei VHF♦︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎-Patient:innen ≥ 75 Jahren. Hier geht es zu den Ergebnissen.
VHF♦︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎︎= nicht-valvuläres Vorhofflimmern
* Schwere Blutung definiert nach den Kriterien der International Society on Thrombosis and Haemostasis (ISTH): tödliche Blutung, Blutung in einem kritischen Bereich oder Organ (intrakranielle, intraspinale, intraokuläre, retroperitoneale, intraartikuläre, oder Perikardblutung oder intramuskuläre Blutung mit Kompartmentsyndrom), Blutung mit einem Hämoglobinabfall ≥ 2 g/dl, Transfusionsbedarf von ≥ 2 Einheiten Erythrozytenkonzentrat/Vollblut).
† Schwere Blutung definiert als klinisch manifeste Blutung assoziiert mit tödlichem Ausgang, Beteiligung eines kritischen anatomischen Bereichs (intrakraniell, spinal, okular, perikardial, artikulär, retroperitoneal oder intramuskulär mit Kompartmentsyndrom), Hämoglobinabfall ≥ 2 g/dL, Transfusion mit ≥ 2 Einheiten Vollblut/Erythrozytenkonzentrat oder permanente Behinderung.
‡ Schwere Blutung definiert als Reduktion des Hämoglobin-Levels um mindestens 2 g/dL, Transfusion von mindestens 2 Einheiten Blut oder unter Erfordernis von inotropen Substanzen, symptomatische Blutungen in kritischem Bereich oder Organ.
£ Relatives Risiko in RE-LY.