BTK-Inhibitor der 2. Generation: Die Selektivität macht den Unterschied?!
Der Unterschied zwischen den verfügbaren Bruton-Tyrosinkinase-Inhibitoren (BTKi) der ersten und zweiten Generation liegt maßgeblich in ihrer Selektivität für die BTK. Diese wurde bei dem BTKi der zweiten Generation gezielt verbessert, mit dem Bestreben die Verträglichkeit und damit den langfristigen Therapieerfolg positiv zu beeinflussen.
Das therapeutische Management bei der chronischen lymphatischen Leukämie (CLL) wird heute durch zielgerichtete Therapien dominiert, während die Chemo(immun)therapie an Bedeutung verloren hat. Dabei nimmt die Inhibition der Bruton-Tyrosinkinase (BTK) einen zentralen Stellenwert ein. BTK-Inhibitoren (BTKi) werden in der aktuellen Onkopedia-Leitlinie über alle Indikationssegmente hinweg als Standardtherapie empfohlen. Seit Ende 20201 steht mit Acalabrutinib (Calquence®) ein BTKi der zweiten Generation zur Verfügung. Calquence® wird als Mono- oder als Kombinationstherapie mit Obinutuzumab bei erwachsenen Patienten mit nicht vorbehandelter CLL eingesetzt, zudem kann der BTKi auch als Monotherapie bei Patienten mit mindestens einer Vorbehandlung eingesetzt werden.
Häufiger Therapieabbruch unter Ibrutinib
Das Toxizitätsprofil von Ibrutinib, dem BTKi der ersten Generation, limitiert seinen Einsatz spürbar. Die Real-World-Evidenz spricht dafür, dass es im Praxisalltag sogar noch häufiger als in den randomisierten klinischen Studien zu einem nebenwirkungsbedingten Absetzen von Ibrutinib kommt. Einer retrospektiven Analyse zufolge bricht fast jeder vierte Patient (23 %)2 eine Ibrutinib-Therapie im realen Behandlungsgeschehen vorzeitig ab, was den Bedarf für einen neuen, verträglicheren BTKi verdeutlicht.
BTKi der 1. und 2. Generation: Unterschiede im selektiven Bindungsverhalten
Die BTK gehört zu den Tyrosinkinasen der Tec-Familie und wird u. a. in B-Lymphozyten, Knochenmarks- und Mastzellen sowie Thrombozyten exprimiert. Als proximale Komponente des B-Zell-Rezeptor-Signalwegs spielt die BTK für die Proliferation und das Überleben der Zellen eine essenzielle Rolle. Sowohl Ibrutinib als auch das neuere Acalabrutinib binden kovalent an das aktive Zentrum der Kinase, was zu einer irreversiblen Hemmung ihrer enzymatischen Aktivität führt.
Auf der inhibierten Signaltransduktion, die überschießendes Zellwachstum verhindert, gründet sich die antineoplastische Wirksamkeit der BTKi bei einer Reihe von B-Zell-Malignitäten, einschließlich der CLL. Da nicht-neoplastische Zellen durch die selektive Interaktion weniger beeinflusst werden, profitieren die Patienten zusätzlich zu den Effektivitätsvorteilen auch von einer besseren Verträglichkeit des BTKi-Regimes gegenüber einer Chemo(immun)therapie.
Im selektiven Bindungsverhalten der verschiedenen BTKi finden sich in vitro relevante Unterschiede: Während Ibrutinib neben der BTK eine Reihe von weiteren Kinasen inhibiert, ist das beim hochselektiven Acalabrutinib nur in einem sehr geringen Ausmaß der Fall. Gegenüber TEC, EGFR, ITK und TXK, bzw. Kinasen der Scr-Familie, weist Acalabrutinib im Unterschied zu Ibrutinib nur eine schwache bzw. keine off target Bindungsaktivität auf. Somit spielen Off-Target-Effekte, die u.a. die T-Zell-Aktivierung, die EGFR-Aktivierung von Epidermalzellen und die Zytotoxizität von NK-Zellen betreffen könnten, unter Acalabrutinib im Gegensatz zu Ibrutinib eine deutlich geringere Rolle.
In-vitro-Ergebnisse zur Kinasehemmung: Acalabrutinib hemmt die BTK selektiver als Ibrutinib3,4
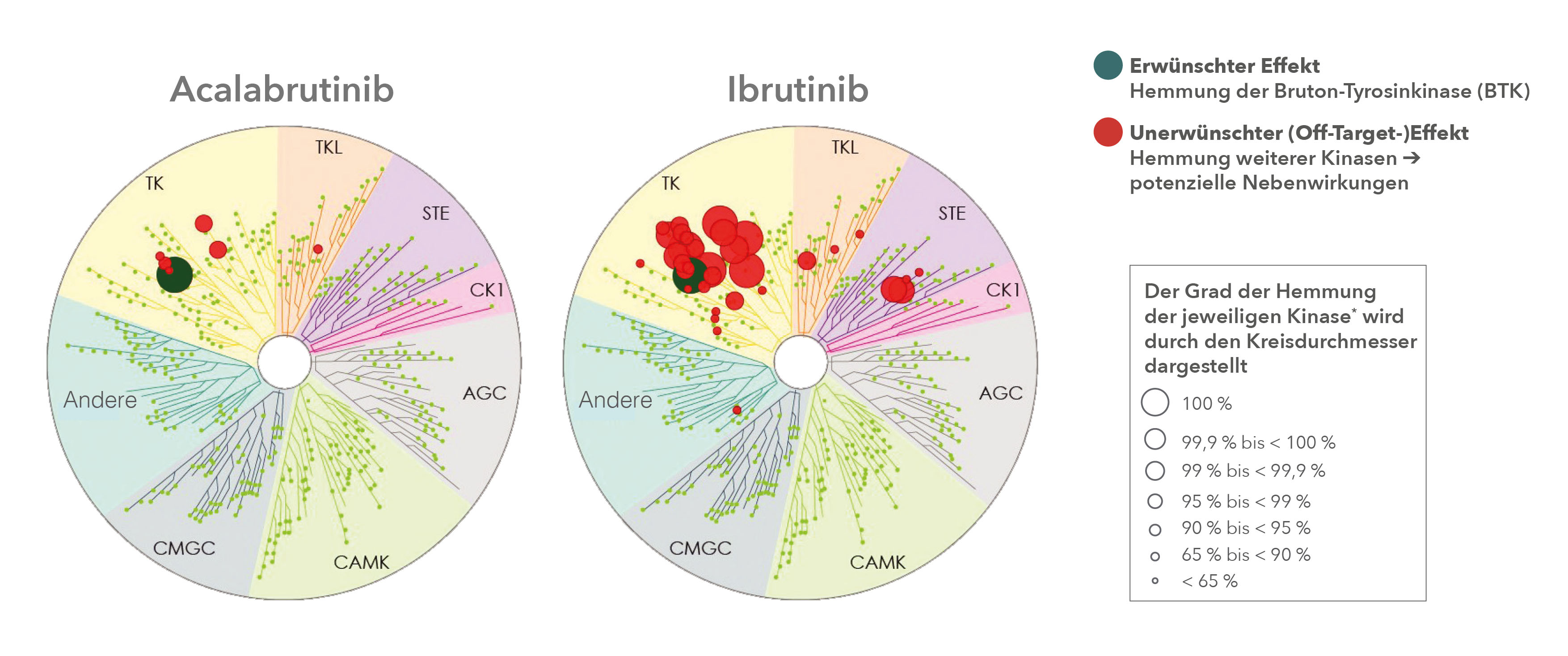
Abbildung adaptiert nach Herman et al 20174: Profil von Acalabrutinib und Ibrutinib in einem kompetitiven Bindungstest mit 395 humanen Kinasen und krankheitsrelevanten Mutanten, bei Testung einer Konzentration von 1 μM im Vergleich zu unbehandelter Kontrolle. (TK = Tyrosinkinasen; TKL = Tyrosinkinase-ähnliche Kinasen, STE = Kinasen mit Ähnlichkeit zu Steril-7, -11 und -20 aus Saccharomyces cerevisiae)
Off-Target-Effekte könnten der Grund für die unterschiedlichen Verträglichkeitsprofile sein
Zu den unter BTKi beobachteten Nebenwirkungen, die möglicherweise durch die Inhibition von Off-Target-Kinasen erklärt werden können, zählen etwa das erhöhte Risiko für Vorhofflimmern, Blutungen, Hautausschlag und Diarrhö.
|
Off-Target-Kinase
|
Möglicher Zusammenhang mit unerwünschten Ereignissen bei Hemmung der jeweiligen Kinase (In-vitro-Daten)3-5,*
|
|
EGFR
|
Hautausschlag, Diarrhö (vermutlich Klasseneffekte)
|
|
ITK
|
Minderung der antikörperabhängigen zellulären Zytotoxizität von NK-Zellen, Reduktion der TH17-T-Zellen
|
|
TXK
|
Einfluss auf das Verhältnis von TH17/Treg-Zellen
|
|
TEC
|
Blutungen
|
|
Kinasen der Src-Familie
|
Blutungen (LCK, SRC) und Vorhofflimmern (CSK)
|
*Die klinische Relevanz dieser Zusammenhänge bedarf noch einer weiteren Bestätigung durch klinische Studien.
Die Erforschung der pharmakokinetischen Eigenschaften von Acalabrutinib erfolgte in verschiedenen Tiermodellen und an menschlichem Gewebe. Die hochselektive Qualität des Zweitgenerations-BTKi wurde dabei u.a. durch zwei Beobachtungen bestätigt: durch anhaltende Gefäßwand-Interaktionen von Thrombozyten-Isolaten (die unter Ibrutinib-Behandlung signifikant reduziert waren) und durch die intakte NK-Zell-vermittelte Zytotoxizität im peripheren Blut von Acalabrutinib behandelten Patienten.
Für die Behandlungspraxis wichtig: Die kurze Plasma-Halbwertszeit und die hohe Selektivität von Acalabrutinib ermöglichen bei zweimal täglicher Einnahme eine nahezu komplette und kontinuierliche BTK-Inhibition von ≥ 95 %6 über 24 Stunden ohne gesteigerte Toxizität aufgrund von hohen Dosispeaks.
Zur Charakterisierung des Nebenwirkungsprofils im therapeutischen Einsatz tragen maßgeblich die Daten aus klinischen Phase-III-Studien bei. In den zulassungsrelevanten Studien ELEVATE-TN8 und ASCEND9 kam es unter Acalabrutinib bei jeweils nur 2 %8,9 der Patienten zu einer Blutung ≥ Grad 3. Zudem waren kardiovaskuläre Nebenwirkungen wie Vorhofflimmern und Bluthochdruck unter Acalabrutinib (ELEVATE-TN8) meist niedriggradig.
Acalabrutinib in ELEVATE TN8: Vorhofflimmern und Bluthochdruck waren meist von Grad 1 und 2
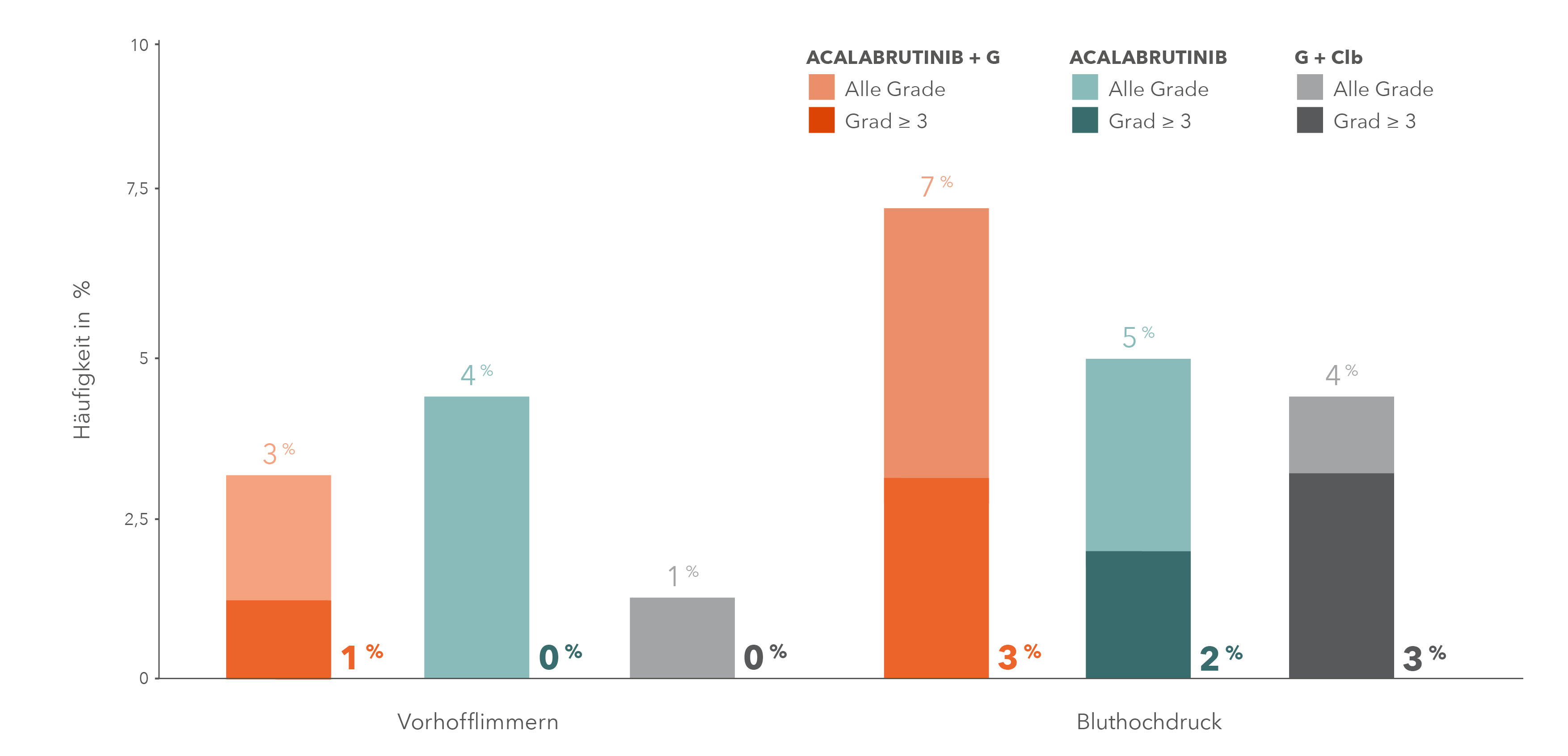
Clb = Chlorambucil; G = Obinutuzumab
Acalabrutinib in ASCEND9: Vorhofflimmern und Bluthochdruck waren meist von Grad 1 und 2
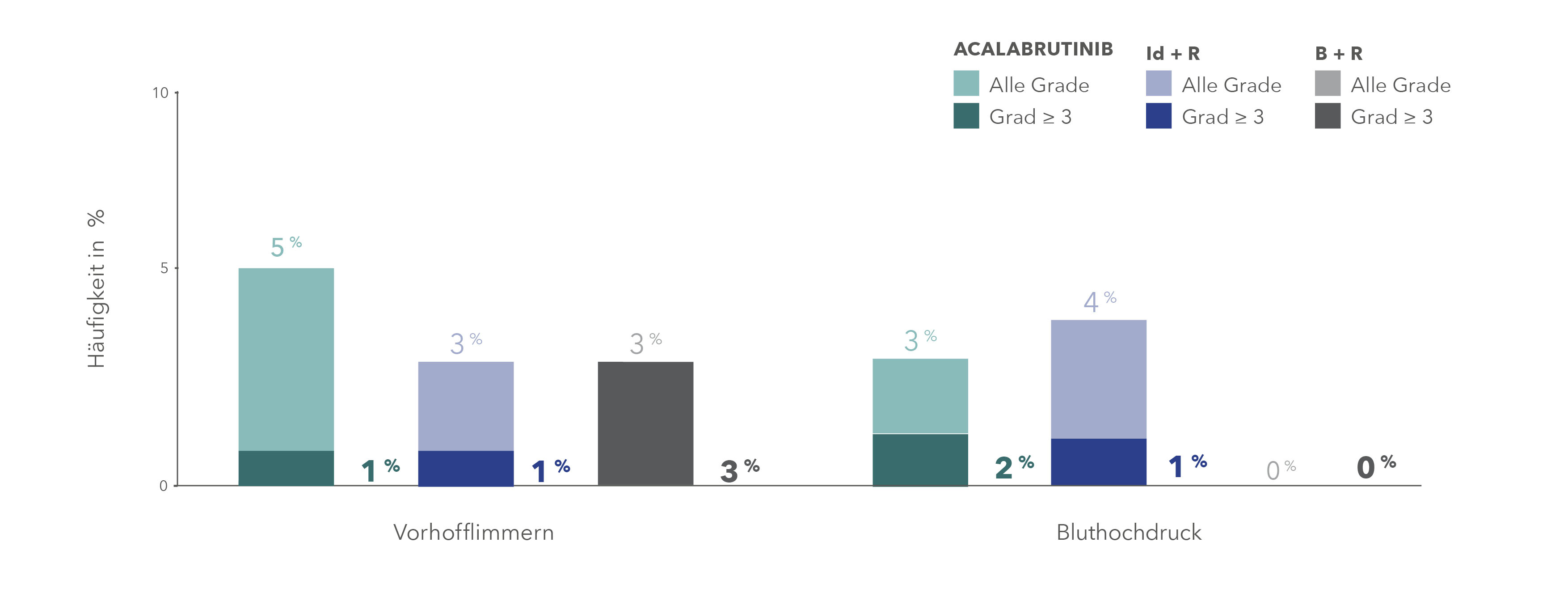
B + R = Bendamustin + Rituximab; Id + R = Idelalisib + Rituximab
Ibrutinib: Raten an Vorhofflimmern und Bluthochdruck in der RESONATE-27-Studie
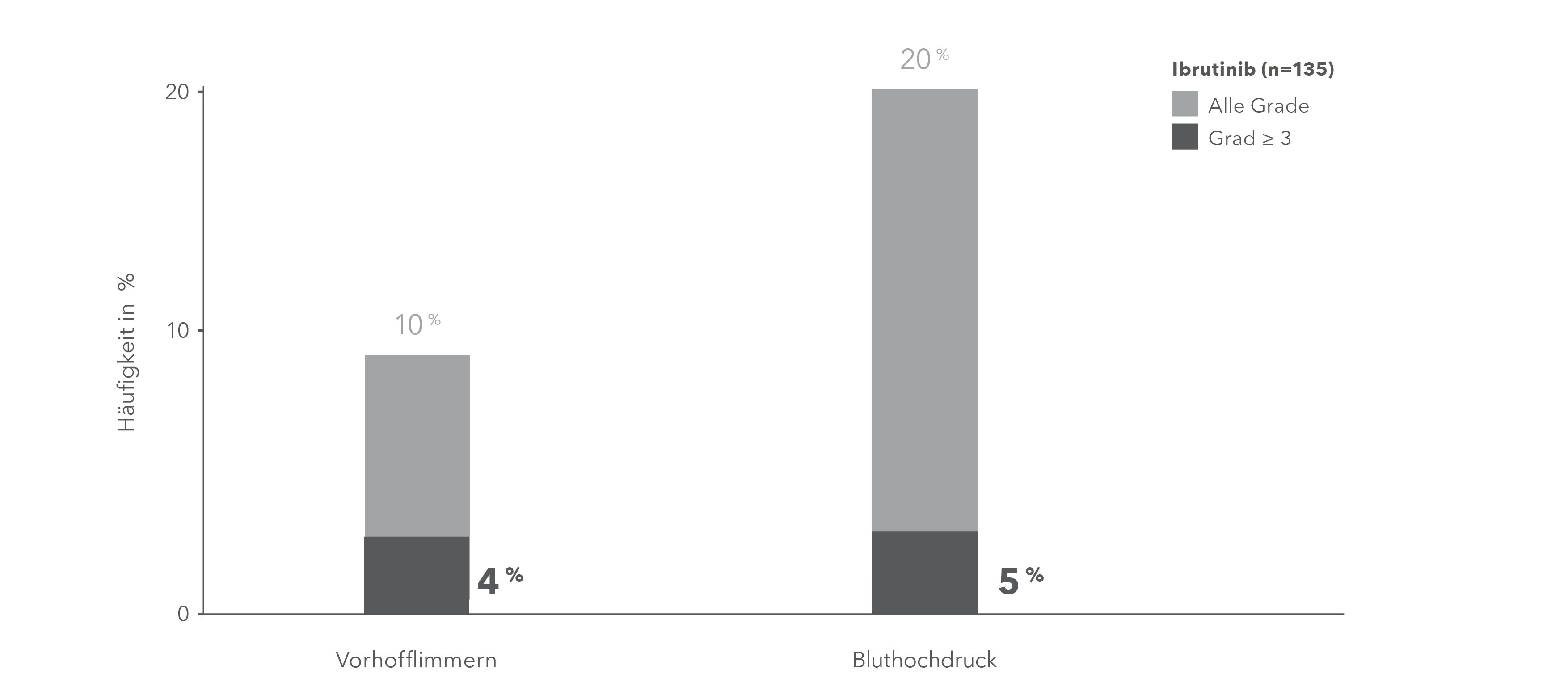
Ibrutinib: Raten an Vorhofflimmern und Bluthochdruck in der iLLUMINATE10-Studie
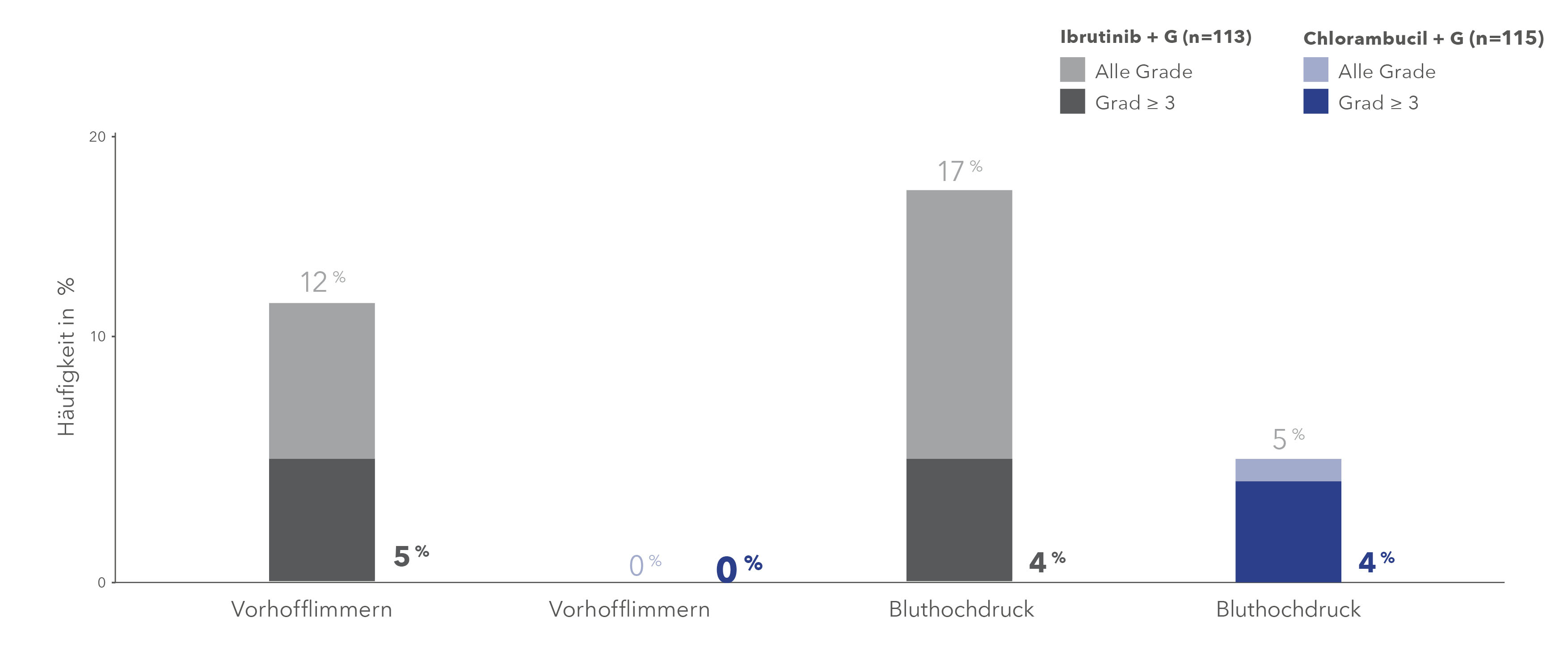
G = Obinutuzumab
Aktuelle Daten bestätigen Vorteile bei der kardiovaskulären Sicherheit
Zwei im Jahr 2019 publizierte Studienergebnisse aus Phase I/II-Studien11,12 belegen eine hohe Ansprechrate und gute Verträglichkeit bei Ibrutinib-intoleranten CLL-Patienten nach Umstellung auf Acalabrutinib. Im Zuge der ASH-Tagung 2020 präsentierte Daten untermauern die Vorteile des Zweitgenerations-BTKi hinsichtlich des kardiovaskulären Sicherheitsprofils. Im Rahmen einer gepoolten Analyse von vier Studien zur Acalabrutinib-Monotherapie brachen lediglich 0,9 %13 der Patienten mit kardiovaskulären Ereignissen die Acalabrutinib-Therapie ab.
Zudem stützt eine Netzwerk-Metaanalyse14 das gute kardiovaskuläre Sicherheitsprofil von Acalabrutinib mit geringeren Raten an Anämien, Thrombozytopenien und kardiovaskulären Nebenwirkungen als unter Ibrutinib. Ergebnisse einer klinischen Head-to-Head-Studie, die Acalabrutinib als BTKi der zweiten Generation direkt mit Ibrutinib vergleicht, werden Mitte diesen Jahres erwartet.
Besondere Relevanz der BTKi in Pandemie-Zeiten
Unter den Bedingungen der COVID-19-Pandemie ist weiterhin und erst recht ein leitliniengerechtes CLL-Management anzustreben, da die Tumorkontrolle auch der Infektkontrolle dient. Expertenempfehlungen fokussieren dabei die BTKi-Monotherapie, die oral appliziert wird und im Regelfall weniger Reiseaktivität bzw. Krankenhausbesuche erfordert, da die Notwendigkeit einer engmaschigen Kontrolle zumeist entfällt. Im Binnenverhältnis der beiden verfügbaren BTKi sind die Verträglichkeitsvorteile von Acalabrutinib bei hoher Wirksamkeit mit Blick auf die Therapieadhärenz von umso höherer Relevanz.
- Fachinformation Calquence®, Stand November 2020
- Sharman JP et al. Understanding Ibrutinib Treatment Discontinuation Patterns for Chronic Lymphocytic Leukemia. Blood 2017;130:4060 (ASH Abstr)
- Barf T et al. Acalabrutinib (ACP-196): A Covalent Bruton Tyrosine Kinase Inhibitor with a Differentiated Selectivity and In Vivo Potency Profile. J Pharmacol Exp Ther 2017;363:240-52
- Herman SEM et al. The Bruton’s tyrosine kinase (BTK) inhibitor acalabrutinib demonstrates potent on-target effects and efficacy in two mouse models of chronic lymphocytic leukemia. Clin Cancer Res 2017;23(11):2831-41
- Xiao L et al. Ibrutinib-Mediated Atrial Fibrillation Attributable to Inhibition of C-Terminal Src Kinase. Circulation 2020;142(25):2443-55
- Byrd JC et al. Acalabrutinib (ACP-196) in relapsed chronic lymphocytic leukemia. N Engl J Med 2016;374:323-32
- Barr PM et al. Sustained efficacy and detailed clinical follow-up of first-line ibrutinib treatment in older patients with chronic lymphocytic leukemia: extended phase 3 results from RESONATE-2. Haematologica 2018;103(9):1502-10
- Sharman JP et al. Acalabrutinib with or without obinutuzumab versus chlorambucil and obinutuzumab for treatment-naive chronic lymphocytic leukaemia (ELEVATE TN): a randomised, controlled, phase 3trial. Lancet 2020;395:1278-91
- Ghia P et al. ASCEND: Phase III, Randomized Trial of Acalabrutinib Versus Idelalisib Plus Rituximab or Bendamustine Plus Rituximab in Relapsed or Refractory Chronic Lymphocytic Leukemia. J Clin Oncol 2020;38(25):2849-61
- Moreno C et al. Ibrutinib plus obinutuzumab versus chlorambucil plus obinutuzumab in first-line treatment of chronic lymphocytic leukaemia (iLLUMINATE): a multicentre, randomised, open-label, phase 3 trial. Lancet Oncol 2019;20:43-6
- Awan FT et al. Acalabrutinib monotherapy in patients with chronic lymphocytic leukemia who are intolerant to Ibrutinib. Blood Adv. 2019;3(9):1553-62
- Rogers K et al. Phase 2 study of acalabrutinib in ibrutinib (IBR)-intolerant patients (pts) with relapsed/refractory (R/R) chronic lymphocytic leukemia (CLL). J Clin Oncol 2019;37(15_suppl):7530
- Brown JR et al. Pooled Analysis of Cardiovascular Events from Clinical Trials Evaluating Acalabrutinib Monotherapy in Patients with Chronic Lymphocytic Leukemia (CLL). ASH 2020, Abstract 3146
- Hilal T et al. Adverse Events in Clinical Trials of Ibrutinib and Acalabrutinib for B-Cell Lymphoproliferative Disorders: A Systematic Review and Network Meta-Analysis. ASH 2020, Abstract 1317
- Study of Acalabrutinib (ACP-196) Versus Ibrutinib in Previously Treated Subjects With High Risk CLL. ClinicalTrials.gov Identifier: NCT02477696. https://clinicaltrials.gov/ct2/show/NCT02477696
Abkürzungen:
ASH = American Society of Hematology
BTKi = Bruton-Tyrosinkinase-Inhibitor
CLL = chronische lymphatische Leukämie
DGHO = Deutsche Gesellschaft für Hämatologie und Medizinische Onkologie
EGFR = Epidermal Growth Factor Receptor (Rezeptor-Tyrosinkinase)
ITK = Interleukin-2-induzierbare T-Zell-Kinase
DE-35069\21




