- Nationale VersorgungsLeitlinie Chronische Herzinsuffizienz – Langfassung, 3. Auflage, Version 3, 2019. doi: 10.6101/AZQ/000482. www.leitlinien.de/herzinsuffizienz.
- McDonagh TA et al. Eur Heart J 2021;42(36):3599–3726.
- Maurer MS et al. Circulation 2017;135(14):1357–1377.
- Sekijima Y et al. Curr Pharm Des 2008;14(30):3219–3230.
- Vasan RS et al. JACC Cardiovasc Imaging 2018;11(1):1–11.
- González-López E et al. Eur Heart J 2015;36(38):2585–2594.
- Grogan M et al. J Am Coll Cardiol 2016;68(10):1014–1020.
- Garcia-Pavia P et al. Eur Heart J 2021;42(16):1554–1568.
- Yilmaz A et al. Clin Res Cardiol 2021;110(4):479–506.
- Maurer MS et al. N Engl J Med 2018;379(11):1007–1016.
Kardiale Amyloidose als Ursache der Herzinsuffizienz – die kardiologische Abklärung ist entscheidend
Scheinbar eindeutige Symptome wie Dyspnoe und mangelnde Belastbarkeit, doch die Behandlung der Herzinsuffizienz zeigt keine Wirkung? Dann ist schnelles Handeln gefragt, denn es könnte eine kardiale Amyloidose dahinterstecken. Welche Schritte führen zur gesicherten Diagnose?
Die Symptome einer Herzinsuffizienz sind in der Regel eindeutig und gut bekannt: Dyspnoe, mangelnde Belastbarkeit, Müdigkeit und Abgeschlagenheit sowie periphere Ödeme sind entscheidende Anzeichen. Nach der durch eine kardiologische Praxis abgeklärten Diagnose einer Herzinsuffizienz wird die medikamentöse Standardtherapie eingeleitet.1,2 Auf den ersten Blick ein klarer Fall!
Neben den häufigsten Ursachen einer Herzinsuffizienz wie der koronaren oder der hypertensiven Herzerkrankung gibt es jedoch weitere Ursachen, die auch in der niedergelassenen Allgemeinarztpraxis nicht vergessen werden dürfen. Vor allem bei Patient:innen mit einer Herzinsuffizienz, bei denen die medikamentöse Standardtherapie keinen hinreichenden Einfluss auf die Symptome zeigt, lohnt es sich, die genaue Ursache zu identifizieren und schnell zu handeln. Denn hinter der Symptomatik einer Herzinsuffizienz kann sich die häufig unterdiagnostizierte, aber ursächlich behandelbare Erkrankung namens Transthyretin-Amyloidose mit Kardiomyopathie (ATTR-CM) verbergen – eine systemische Speichererkrankung, die durch Bildung und Ablagerung von Amyloidfibrillen verursacht wird.3,4
Aufgrund ihrer schlechten Prognose mit hoher Morbidität und Mortalität muss deshalb das Augenmerk auf eine frühzeitige Diagnose gelegt werden, zumal die Erkrankung häufiger vorzukommen scheint als bisher gedacht: Studien zeigen, dass bei bis zu 13,3 % der Patient:innen mit Herzinsuffizienz mit erhaltener Pumpfunktion (HFpEF) eine ATTR-CM nachgewiesen werden kann.5–7 Mit der gesicherten Diagnose ATTR-CM kann schließlich auch die krankheitsmodifizierende Kausaltherapie eingeleitet werden.
Doch welche Schritte führen zur gesicherten Diagnose? Bei der Diagnose ist es entscheidend, den Blick sowohl für kardiale als auch extrakardiale Symptome und Anzeichen zu schärfen. Denn wenn es einfach nicht zusammenpasst, dann muss bei Herzinsuffizienz-Patient:innen auch an eine ATTR-CM gedacht werden:8,9
- Keine Verbesserung nach Therapieeinstellung auf Standard-Herzinsuffizienz-Therapie
- Männlich und (beidseitiges) Karpaltunnelsyndrom
- NT-proBNP deutlich über Normwerten (> 125 pg/ml)
- Auffälligkeiten im EKG (siehe Abbildung):
- Niedervoltage ↘
- Pseudoinfarktmuster ↗
- Vorhofflimmern
- AV-Block
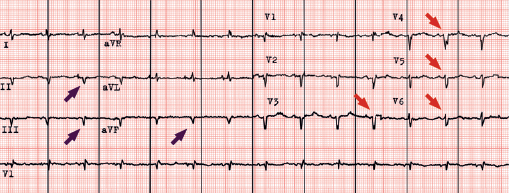
Neben den Auffälligkeiten im EKG ist bei der frühzeitigen Erkennung der ATTR-CM auch die Echokardiografie von zentraler Bedeutung.1,2 Die aktuelle Nationale VersorgungsLeitlinie Chronische Herzinsuffizienz empfiehlt mit dem höchsten Empfehlungsgrad „soll“ bei allen Patient:innen, bei denen nach der Basisdiagnostik der Verdacht auf Herzinsuffizienz weiterhin besteht, eine zeitnahe Durchführung einer transthorakalen Echokardiografie.1
Deshalb ist bereits bei Verdacht auf Herzinsuffizienz die kooperative und interdisziplinäre Zusammenarbeit mit Kardiolog:innen zur Abklärung der Herzinsuffizienz-Ursache und Absicherung der Diagnose wichtig, da den Fachärzt:innen neben dem EKG mit Echokardiografie und kardialer Magnetresonanztomografie weitere unterstützende bildgebende Maßnahmen zur Verfügung stehen.
Der echkardiografische Befund einer verdickten Herzwand ≥ 12 mm ist eine weitere Red Flag für eine ATTR-CM.8,9
Die Überweisung der Patient:innen an eine kardiologische Praxis sowie die Zusammenarbeit und Kommunikation zwischen Patient:innen, Haus- und Fachärzt:innen sind für eine bessere Prognose entscheidend, um die frühzeitige Diagnose und Einleitung der krankheitsmodifizierenden Kausaltherapie sicherzustellen.10
Der eindringliche Appell lautet deshalb:
Handeln Sie schnell, denn die ATTR-CM ist mit einer hohen Morbidität und Mortalität assoziiert: Die mediane Überlebenszeit nach Diagnose liegt ohne Behandlung bei etwa 3,6 Jahren.7 Eine umgehende kardiologische Abklärung wird deshalb bei Verdacht auf eine ATTR-CM als Ursache der Herzinsuffizienz dringend empfohlen.