Neue Studiendaten zu Vyndaqel<sup>®</sup> 61mg* aus bis zu 7 Jahren Nachbeobachtungszeitraum<sup>1,#</sup>
Eine aktuelle Post-hoc-Analyse der ATTR-ACT-Studiendaten und der Langzeitverlängerung (Follow-Up bis zu 90 Monate)<sup>+,1</sup> zeigte über bis zu 7 Jahren einen Vorteil von Vyndaqel<sup>®</sup> 61 mg* bei der Behandlung von ATTR-CM in den NAC-Stadien I/II gegenüber der von Placebo auf Vyndaqel<sup>®</sup> gewechselten Gruppe.<sup>#,1</sup>
Vyndaqel® (Tafamidis) 61 mg* reduziert über bis zu 7 Jahre+ signifikant die Gesamtmortalität sowie CV-bedingte Mortalität bei ATTR-CM-Patient:innen im NAC-Stadium I & II – und zeigte bei NAC-Stadium III einen positiven Trend gegenüber der von Placebo auf Vyndaqel® gewechselten Gruppen.‡,#,1
Direkt zur Studie von Damy et al.
Die Kernergebnisse auf einen Blick
Vergleich der Gesamtmortalität von Patient:innen, die kontinuierlich Tafamidis 80/61mg* erhielten vs. Placebo zu Tafamidis 80/61mg* nach NAC-Stadium zum EOS:
NAC I: Reduktion der Gesamtmortalität um 57 % (p < 0,001)
NAC II: Reduktion der Gesamtmortalität um 49 % (p = 0,003)
NAC III: Reduktion der Gesamtmortalität um 25 % (p = 0,298)
Gesamtmortalität bei ATTR-CM-Patient:innen im NAC Stadium I, die Vyndaqel 80/61mg* erhielten oder von Placebo zu Vyndaqel 80/61mg* gewechselt sind:
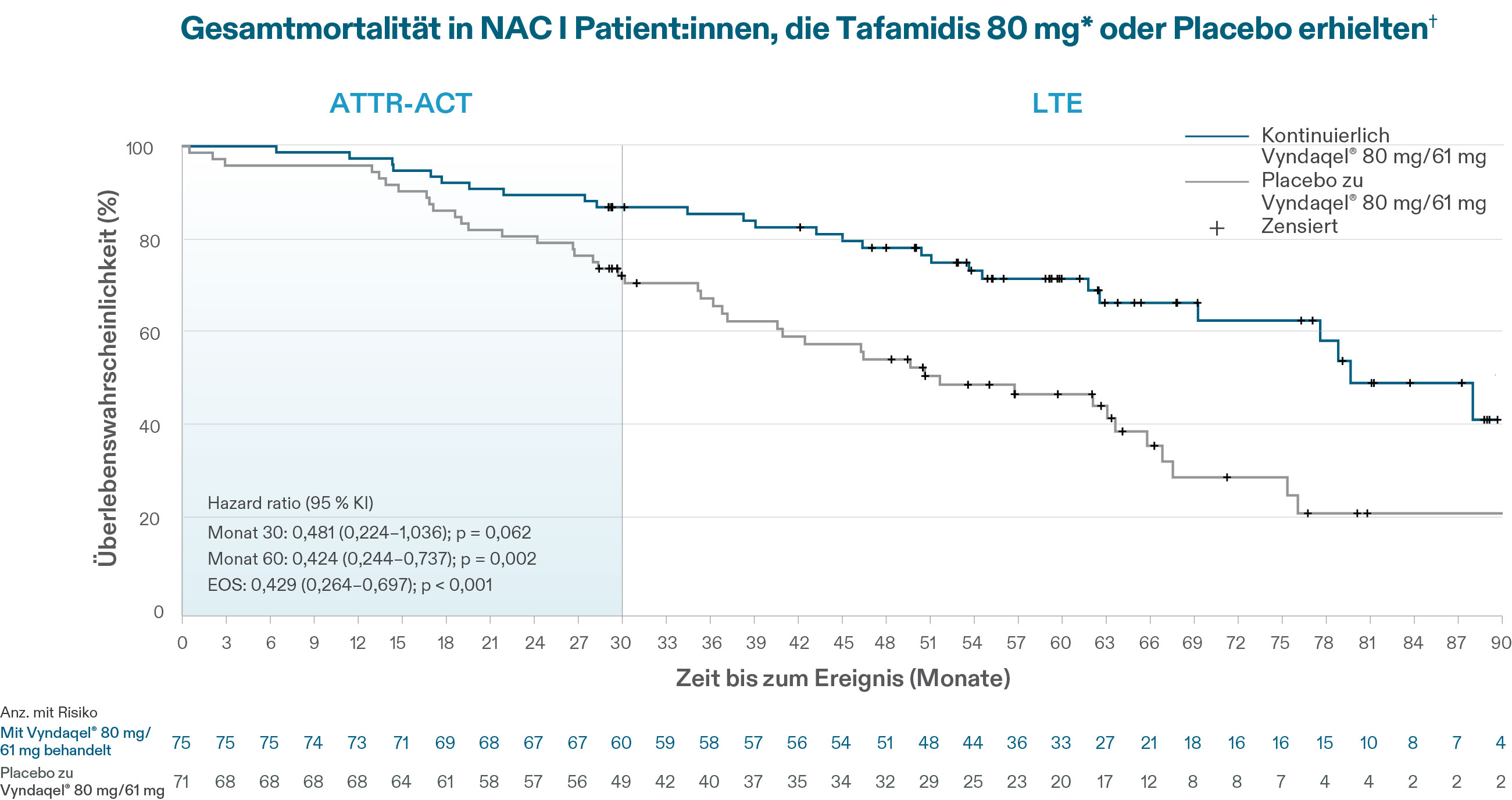
Die kontinuierliche Behandlung mit Vyndaqel® (Tafamidis) 80/61 mg* reduzierte die Gesamtmortalität sowie die CV-bedingte Mortalität in den NAC-Stadien I und II signifikant gegenüber der von Placebo auf Vyndaqel® gewechselten Gruppen.# Dies unterstreicht die Bedeutung einer frühzeitigen Diagnose und Therapieeinleitung.1
Mehr zu Vyndaqel® 61 mg erfahren
Abkürzungen:
ATTR-ACT = klinische Studie mit Tafamidis bei Transthyretin-Kardiomyopathie
ATTR-CM = Transthyretin-Amyloidose mit Kardiomyopathie
CV = Kardiovaskulär; eGFR = geschätzte glomeruläre Filtrationsrate
EOS = end of study
KI = Konfidenzintervall
LTE = long-term extension
NAC = National Amyloidosis Centre
NT-proBNP = N-terminales natriuretisches Peptid Typ B
# Weder ATTR-ACT noch die LTE-Studie waren statistisch darauf ausgelegt, die Wirkung von Tafamidis 80/61 mg* nach NAC‑Stadium zu untersuchen; daher sind die Ergebnisse explorativ.1
* Vyndaqel® (Tafamidis) 61 mg und Vyndaqel® (Tafamidis-Meglumin) 80 mg sind indiziert zur Behandlung der Wildtyp oder hereditären Transthyretin-Amyloidose bei erwachsenen Patient:innen mit Kardiomyopathie.2 Eine einzelne Kapsel Vyndaqel® 61 mg ist bioäquivalent zu Vyndaqel® 80 mg (vier Kapseln zu 20 mg). Diese sind auf Basis der mg-Angabe nicht gegeneinander austauschbar.2,3
+ Die Endpunkte wurden über einen Nachbeobachtungszeitraum von bis zu 90 Monaten bewertet. Zum Abschluss der Studie betrug die mediane Nachbeobachtungsdauer bei Patient:innen mit einem NAC‑Stadium I zu Studienbeginn 63 Monate (kontinuierlich Tafamidis 80/61 mg*) bzw. 64 Monate (Placebo zu Tafamidis 80/61 mg*). Die entsprechende mediane Nachbeobachtungsdauer bei Patient:innen der einzelnen Behandlungsgruppen mit NAC‑Stadium II bzw. III zu Studienbeginn betrug 61 und 59 Monate sowie 52 und 53 Monate.1
‡ NAC I: NT‑proBNP ≤ 3.000 ng/l und gleichzeitig eGFR ≥ 45 ml/min/1,73m2;1
NAC II: NT-proBNP >3000 ng/l oder eGFR <45 ml/min/1.73 m2;1
NAC III: NT‑proBNP > 3.000 ng/l und gleichzeitig eGFR < 45 ml/min/1,73m2;1
- Damy T et al. Eur J Heart Fail. Published online June 9, 2025.
- Fachinformation Vyndaqel® 61 mg, aktueller Stand.
- Lockwood PA et al. Clin Pharmacol Drug Dev. 2020;9(7):849–854.
PP-VYN-DEU-4558
