a Olumiant® (Baricitinib) wird angewendet zur Behandlung von mittelschwerer bis schwerer aktiver rheumatoider Arthritis bei erwachsenen Patienten, die auf eine vorangegangene Behandlung mit einem oder mehreren krankheitsmodifizierenden Antirheumatika (DMARD) unzureichend angesprochen oder diese nicht vertragen haben. Baricitinib kann als Monotherapie oder in Kombination mit Methotrexat angewendet werden.
b Rheumatoide Arthritis: Beobachtung der Biologika-Therapie
c American College of Rheumatology; Verbesserung um mindestens 20 % bei definierten ACR-Kriterien
d Nach 7 Jahren erreichten die verbleibenden Patienten (21,5 %, bei Studienstart n=808) eine Remission, vgl. insb.: 56–66 % gemessen am DAS28-hsCRP, 28–30 % gemessen am SDAI, 29–34 % gemessen am CDAI. Daten nicht gezeigt für Patientengruppen, die in den Ausgangsstudien auf Placebo oder Adalimumab randomisiert wurden.4
e Disease Activity Score 28-Joint Count High-Sensitivity C-reactive Protein
f Hierbei handelt es sich um Daten aus der Behandlungsrealität, die nicht in randomisierten, kontrollierten und konfirmatorischen Studien, sondern ergänzend zu diesen Daten erhoben wurden.
g Für diese Patientenpopulationen gelten besondere Warnhinweise und Vorsichtsmaßnahmen laut aktueller Fachinformation: Patienten mit atherosklerotischen Herz-Kreislauferkrankungen oder kardiovaskulären Risikofaktoren, Patienten mit Risikofaktoren für maligne Erkrankungen, Patienten ab 65 Jahren und Patienten mit aktiven, chronischen bzw. wiederkehrenden Infekten in der Vorgeschichte.1
h Major Adverse Cardiac Event; unerwünschte kardiovaskuläre Ereignisse
i conventional synthetic Disease-Modifying Antirheumatic Drug (konventionell krankheitsmodifizierende Antirheumatika)
j Baricitinib sollte bei Patienten ≥ 65 Jahre nur angewendet werden, wenn keine geeignete Behandlungsalternative zur Verfügung steht.1
k Biological/targeted synthetic Disease-Modifying Anti-rheumatic Drug (biologisches/zielgerichtetes krankheitsmodifizierendes Antirheumatikum)
l Clinical Disease Activity Index
m venöse Thromboembolien
DGRh 2023 – Neues aus Klinik und Praxis: JAKi vor TNFi?
Prof. Dr. Ulf Müller-Ladner (Bad Nauheim), Prof. Dr. Eugen Feist (Vogelsang-Gommern) und Prof. Dr. Hendrik Schulze-Koops (München) diskutierten auf dem 51. DGRh-Kongress in Leipzig, welche klinische Perspektive Januskinase (JAK)-Inhibitoren in der Langzeittherapie der rheumatoiden Arthritis (RA)<sup>a</sup> bieten.
Klinische Perspektive: JAK-Inhibitoren in der Langzeittherapie
Prof. Dr. Ulf Müller-Ladner schilderte anhand des RABBITb-Registers, dass seit Zulassung der JAK-Inhibition in 2017 der Einsatz der Substanzklasse stark angestiegen ist.
Für eine erfolgreiche Langzeittherapie und damit einhergehende anhaltende Adhärenz gelten laut Prof. Ladner folgende Parameter als wichtig:
- a.) Klinisches Ansprechen nach Standard-Scores:
- Bereits in der Zulassungsstudie RA-BEAM erwies sich Baricitinib1 im direkten Vergleich beim Erreichen des primären Endpunktes (ACR20-Ansprechratec in Woche 12) dem TNF-Inhibitor Adalimumab als signifikant überlegen (70 % mit Baricitinib vs. 61 % mit Adalimumab, p ≤ 0,05).2 Daten aus dem Versorgungsalltag untermauern die Wirksamkeit aus den klinischen Studien und zeigen, dass mit einer Therapie mit einem JAK-Inhibitor nach 12 Monaten eine geringe Krankheitsaktivität erzielt werden kann.3 Auch können mit Baricitinib langanhaltende Remissionsraten erreicht werden: In der Verlängerungsstudie RA-BEYOND war auch nach 7 Jahrend mehr als die Hälfte der verbleibenden Studienteilnehmenden (21,5 %) weiterhin stabil in Remission (gemäß DAS28-hsCRPe Kriterien).4
- b.) Schmerzreduktion und Patient:innen-Einschätzung:
- Mit Blick auf die Schmerzbewertung gibt es Unterschiede zwischen Patient:innen- und Ärzt:innen-Perspektive – so spielt, im Unterschied zu Behandelnden, der Schmerz für Patient:innen die größte Rolle bei der Wahrnehmung der Krankheitsaktivität.5 Baricitinib zeigte in klinischen Studien eine starke Wirkung auf den Schmerz: Bereits nach einer Woche berichtete mehr als ein Viertel der Patient:innen von einer Schmerzreduktion um mindestens 50 %.6 Nach 12 Wochen erreichte bereits mehr als die Hälfte mit Baricitinib eine Schmerzreduktion um 50 % und damit signifikant mehr als mit Adalimumab (57 % vs. 49 %; p < 0,05).6 Ebenfalls überzeugte Baricitinib im Direktvergleich mit Adalimumab mit rascher und anhaltender Verbesserung der körperlichen Funktion.2
- c.) Sicherheit:
- Es gibt umfassende Langzeitdaten zur Sicherheit von Baricitinib: So bestätigen die Ergebnisse von 9 klinischen Studien und einer Langzeitverlängerungsstudie im dokumentierten Zeitraum von bis zu 9,3 Jahren ein ausgewogenes Sicherheitsprofilf.7 Die Inzidenzraten (IR) für unerwünschte Ereignisse blieben über den gesamten Zeitraum stabil und waren dabei vergleichbar mit der RA-Population.7,8 Diese Ergebnisse werden durch Real-World Daten (RWD)g untermauert, wie Prof. Ladner vorstellte: Eine Auswertung aus dem RABBIT-Register verglich die IR von Malignomen bei RA-Patient:innen unter JAK-Inhibitoren- mit denen unter TNFi-Therapie. Dabei gab es keine erhöhte IR für Malignome bei JAK-Inhibitor- im Vergleich zu TNFi-behandelten Patient:innen.9 Dies konnte bestätigt werden, obwohl die mit JAK-Inhibitoren behandelten Patient:innen sowohl ein höheres Durchschnittsalter als auch eine längere Krankheitsgeschichte aufwiesen als jene Patient:innen in TNFi-Behandlung. Eine Analyse der JAK-POT-Studie zeigte im Vergleich zu TNFi zudem, dass kein signifikant höheres Risiko von MACEh bei mit JAK-Inhibitoren behandelten RA-Patient:innen vorlag.10
Neues von JAK-Inhibitoren aus dem Praxisalltag
Neben klinischen Daten zu Baricitinib gibt es inzwischen umfassende RWE-Erfahrungen weltweit, welche die starke Wirksamkeit und Sicherheit des JAK-Inhibitors untermauern.
Umfassende RWD zur Wirksamkeit
Prof. Dr. Eugen Feist ging auf jüngst auf dem EULAR-Kongress präsentierte Auswertungen ein, nach denen mit Baricitinib im Versorgungsalltag noch höhere Remissionsraten oder eine niedrige Krankheitsaktivität erreicht werden können als die klinischen Studien (RA-BEAM, RA-BEACON) gezeigt hatten (s. Abb. 1).11,12
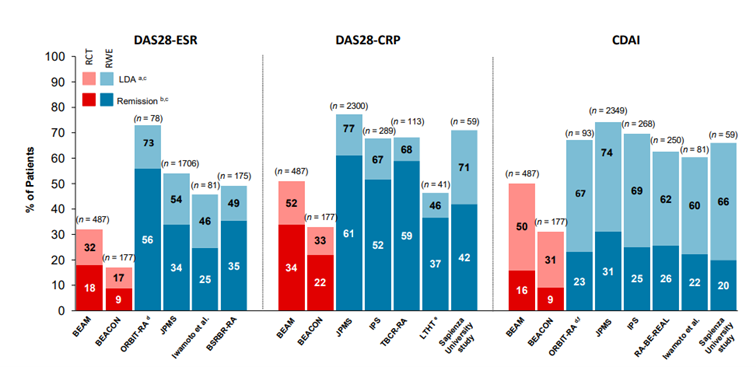
Abb. 1: Treat-to-target: Remission und Low-Disease-Activity (LDA) unter Baricitinib aus RWE und RCTs bei Patient:innen mit RA nach 6 Monaten.11,12
Anschließend widmete sich Prof. Feist einer weiteren auf dem EULAR-Kongress veröffentlichten Auswertung. Die multizentrische, offene Nicht-Unterlegenheits-Studie PERFECT-RA untersuchte die Wirksamkeit von Baricitinib (gemessen anhand des ACR50- und DAS28-Ansprechens) im Vergleich zu TNFi bei RA-Patient:innen mit unzureichendem Ansprechen auf csDMARDsi.13
- Nach 12 Wochen zeigte sich Baricitinib im Hinblick auf das ACR50-Ansprechen als nicht unterlegen und statistisch überlegen gegenüber TNFi.
- Darüber hinaus befanden sich nach 12 Wochen 74 % der Baricitinib-Patient:innen, aber nur 46 % der TNFi-Patient:innen in Remission (definiert als DAS28-CRP < 2,6). Dieses Ansprechen konnte auch über 48 Wochen erhalten bleiben.
Zudem bescheinigt eine weitere auf dem EULAR-Kongress präsentierte, europaweite Auswertung aus dem Versorgungsalltag, dass Baricitinib auch in Monotherapie stark wirksam sein kann. Die Ergebnisse stellte Prof. Feist vor:12 RA-Patient:innen erhalten in der klinischen Praxis Baricitinib häufig in Monotherapie. Etwa 40–78 % der Patient:innen erreichten nach bis zu einem Jahr eine niedrige Krankheitsaktivität oder eine Remission.
Prof. Feist skizzierte darüber hinaus anhand der aktuellen 2-Jahres-Auswertung der RA-BE-REALc, dass anhaltende Remissionsraten mit Baricitinib auch in der Praxis erreicht werden können:14 Unabhängig davon, ob die Studienteilnehmenden über 65 Jahre altj und/oder b/tsDMARDk-erfahren waren, konnten sie unter Baricitinib nach 2 Jahren konsistente CDAIl-Remissionsraten oder eine niedrige Krankheitsaktivität aufweisen. Ebenfalls zeigte sich eine anhaltende Adhärenz, wie auch bereits aus früheren Register-Daten bekannt.2,14
Zudem legt eine Studie aus Erlangen („BAREBONE“; n=27) nahe, dass Baricitinib die funktionellen Eigenschaften des Knochens verbessern kann, wie Prof. Feist erläuterte.15 In dieser Studie wurde die Veränderung der Knochenfestigkeit unter Baricitinib anhand von Scans der Speiche zu Studienbeginn, in Woche 24 und Woche 52 untersucht. Die Ergebnisse demonstrieren, dass sich unter Baricitinib nicht nur die kortikale Porosität verringerte, sondern auch die Widerstandsfähigkeit des Knochens gegen mechanische Belastung verbesserte, was auf eine osteoprotektive Wirkung hinweisen könnte.15
Sicherheit in RWD untermauert
Neben Daten zur Wirksamkeit bieten RWD umfassende Ergebnisse zur Sicherheit. So zeigt die 2-Jahres-Auswertung der RA-BE-REAL: Die Abbruchraten bei Baricitinib-Patient:innen waren unabhängig von Alter oder vorheriger Behandlung nach 2 Jahren ähnlich.14
Weiterhin umriss Prof. Feist die Sicherheit von Baricitinib bzgl. MACE durch unterschiedliche RWD.
- Laut einer Auswertung aus dem deutschen RABBIT-Register ergab der Vergleich von mit JAK-Inhibitoren zu mit TNFi behandelten RA-Patient:innen keine erhöhten MACE-IR bei JAK-Inhibitor-behandelten Patient:innen.16
- Auch eine Kohortenstudie aus Frankreich mit über 14.000 Patient:innen zeigte, dass unter einer JAK-Inhibitor-Therapie kein signifikant erhöhtes Risiko von MACEs und VTEsm im Vergleich zu einer Adalimumab-Therapie vorlag.17
- Ebenfalls präsentierte der Experte eine Analyse der JAK-POT-Studie, welche demonstrierte, dass kein signifikant höheres Risiko von MACE bei RA-Patient:innen, die mit JAK-Inhibitoren behandelt wurden, im Vergleich zu TNFi besteht.10
Frühzeitiger Einsatz: JAKi vor TNFi?
Warum ein frühzeitiger Einsatz und eine rechtzeitige Therapie bei der Behandlung der RA von großer Bedeutung ist, schilderte Prof. Schulze-Koops. Es gibt einen kritischen Zeitraum für den Beginn einer antirheumatischen Therapie. Dieses therapeutische Zeitfenster liege früh im Verlauf der RA und biete bis zu 5 Jahre lang einen anhaltenden Nutzen für die radiologische Progression, so Prof. Schulze-Koops. Die rechtzeitige Einleitung einer antirheumatischen Therapie bei RA-Patient:innen kann daher den langfristigen Krankheitsverlauf verändern.18,19
Warum der Einsatz von JAK-Inhibitoren auch vor TNFi sinnvoll sein kann, erläuterte Prof. Schulze-Koops anhand verschiedener Aspekte. Zu den heranzuziehenden Punkten bei der Entscheidung des frühzeitigen Einsatzes einer spezifischen medikamentösen Therapie gehören laut dem Experten allgemeine Aspekte, wie Zulassungsstatus und Leitlinien bzw. Empfehlungen und Rahmenbedingungen, aber auch individuelle Aspekte, wie die Berücksichtigung der individuellen Risiken, Wirksamkeit, Nebenwirkungen und Komorbiditäten sowie die Art der Anwendung und auch der Patient:innen-Wunsch im Sinne des „Shared-Decision-Making“.
Als wichtige individuelle Aspekte bei der Überlegung hinsichtlich einer spezifischen medikamentösen Therapie nannte Prof. Schulze-Koops:
- Um Erfahrungen und individuelle Risiken zu berücksichtigen, könne die Checkliste der DGRh helfen. Diese kann bei jeder Visite herangezogen werden, Alternativen können besprochen werden und es kann individuell entschieden werden, ob eine Weiterbehandlung mit dem Medikament erfolgen sollte.
- Ebenfalls berücksichtigt werden sollte der individuelle Patient:innen-Wunsch im Sinne des „Shared-Decision-Making“, denn Patient:innen haben das Recht, beispielsweise bei Spritzenphobie/Unfähigkeit zum Spritzen oder MTX-Unverträglichkeit, eine alternative Therapie zu erhalten.
- JAK-Inhibitoren zeigen eine starke Wirksamkeit, wie Prof. Schulze-Koops am Beispiel einer Zulassungsstudie zu Baricitinib zeigte.2 Auch können Remissionsraten über einen langen Zeitraum von 7 Jahren aufrechterhalten werden.4
- Zudem nannte Prof. Schulze-Koops, dass die gute Steuerbarkeit durch Halbwertzeiten von 3 bis 8 Stunden positiv sein kann.1
- Nicht zuletzt ist auch eine anhaltende Adhärenz für den langfristigen Therapieerfolg von hoher Relevanz. Ergebnisse aus dem Versorgungsalltag zeigen, dass dies mit JAK-Inhibitoren ein realistisches Ziel sein kann, so Schulze-Koops.
Prof. Schulze-Koops fasste zusammen, dass es viele Aspekte gäbe, die bei der Therapie-Entscheidung einer Behandlung der RA berücksichtigt werden sollten. Dafür sei auch eine gute Dokumentation wichtig, wobei die DGRh-Checkliste helfen könne. Dabei sei es auch wichtig, mit den Patient:innen die Therapie-Optionen zu besprechen, denn eine effektive Behandlung der RA stünde an erster Stelle.
Fußnoten
Quellen
- Aktuelle Fachinformation Olumiant®
- Taylor PC et al. N Engl J Med 2017;376(7): 652-662 (and supplemental appendix).
- Lauper K et al. Ann Rheum Dis 2022;81:1358–1366.
- Caporali R et al. Ann Rheum Dis 2022;81: 630–631.
- Studenic P et al. Arthritis Rheum 2012;64:2814–23.
- Taylor PC et al. J Clin Med 2019;8 (6): 831.
- Taylor PC et al. Ann Rheum Dis 2022;81: 335.
- Bieber T et al. Adv Ther 2022;39: 4910-60.
- Schaefer M et al. Ann Rheum Dis 2023;82(Suppl):143.
- Aymon R et al. Ann Rheum Dis 2023;82(Suppl):143.
- Taylor PC et al. J Clin Med 2023, 12(13), 4527; https://doi.org/10.3390/jcm12134527.
- Edwards CJ et al. Ann Rheum Dis 2023;82 (suppl 1):1419.
- Oude Voshaar MAH, et al. Ann Rheum Dis 2023;83 (suppl 1):713.
- Alten R et al. Ann Rheum Dis 2023;82 (suppl 1):724-725.
- Simon D et al. Arthritis Rheumatol 2023; doi: 10.1002/art.42617.
- Meissner Y et al. Ann Rheum Dis 2022;81 (Suppl 1):86-87.
- Hoisnard L et al. Ann Rheum Dis. 2022; Epub ahead of print, doi: 10.1136/ard- 2022–222824.
- Egsmose C et al. J Rheumatol 22:2208-13, 1995.
- Finckh A et al. Arthritis Rheum 55:864–72, 20052023;15:1–9.
PP-BA-DE-3860