- Wirksamkeit und Verträglichkeit von Taltz® (Ixekizumab) wurden in einer direkten Vergleichsstudie gegen den TNFα-Blocker Adalimumab (Humira®) untersucht.
- Eingeschlossen waren insgesamt 566 Patientinnen und Patienten mit aktiver Psoriasis-Arthritis und Plaque-Psoriasis mit einer BSA (Body Surface Area) von ≥ 3 %, die zuvor noch mit keinem bDMARD oder JAK(Januskinase)-Inhibitor behandelt wurden (bDMARD-naiv).
- Primärer Endpunkt der Studie war das gleichzeitige Erreichen eines ACR50-Ansprechens, d. h. eine Reduktion der rheumatischen Krankheitsaktivität um mindestens 50 %, und einer vollständig erscheinungsfreien Haut (PASI 100) in Woche 24.
Ist alles Gold was glänzt? Sind TNFi als Goldstandard für die PsA Therapie noch zeitgemäß?
Patient:innen mit Psoriasis-Arthritis<sup>+</sup> (PsA) leiden an vielseitigen Symptomen. Können TNF-Inhibitoren ausreichend helfen? Lesen Sie hier, wie Sie mit dem IL-17Ai Taltz<sup>®1</sup> die PsA-Domänen Gelenke und Haut gleichzeitig wirksam behandeln können.
Eine Psoriasis-Arthritis+ (PsA) kann sich äußerst komplex manifestieren, sodass Betroffene oft an vielen Symptomen gleichzeitig leiden. Das Erscheinungsbild kann dabei von Patient:in zu Patient:in deutlich variieren, was die Diagnosefindung erschwert. Neben den schmerzenden Gelenken schränken auch Hautplaques, Enthesitis, Daktylitis und Nagelpsoriasis die Patientinnen und Patienten stark in ihrem Alltag ein.2
Das Problem: Manchmal vergehen Jahre, bis die endgültige Diagnose gestellt wird. Als gesichert gilt sie meist erst dann, wenn die charakteristischen Haut- und Nagelveränderungen sichtbar sind und der Rheumafaktor im Blut nicht nachweisbar ist.3
Bringt die Diagnose die erhoffte Hilfe?
Steht die Diagnose, legen die Betroffenen große Hoffnung in die Behandlung all ihrer Symptome, um ihrem Leidensweg endlich ein Ende zu setzen. Die Realität sieht in der Praxis aber oft anders aus: Viele Patient:innen erhalten entgegen der aktuellen Leitlinienempfehlungen zu lange Therapien auf Basis von NSAR und/oder klassischen DMARDs.
Das Resultat: Die Behandlung ist in vielen Fällen nicht ausreichend, da die Symptome nicht vollumfänglich adressiert werden. Die Betroffenen erfahren keine zufriedenstellende Verbesserung.
Die aktuellen Empfehlungen sehen bei axialer PsA einen frühzeitigen Einsatz von TNF-Inhibitoren oder Il-17A-Inhibitoren vor, um Langzeitschäden entgegenzuwirken.4 Denn eine rasche Krankheitsprogression kann zu irreversiblen Knochenveränderungen führen, die es zu vermeiden gilt.4
Können alle Domänen gleichzeitig behandelt werden?
Die Suche nach einer Therapie, die mindestens die beiden wichtigsten Domänen Gelenke und Haut wirksam behandeln kann, beschäftigt viele Behandelnde. Denn jede zusätzlich verbesserte Domäne kann die Lebensqualität der Betroffenen erhöhen.
Taltz® zeigt sich gegenüber Adalimumab überlegen im gleichzeitigen Ansprechen auf Gelenk- und Hautsymptome.5
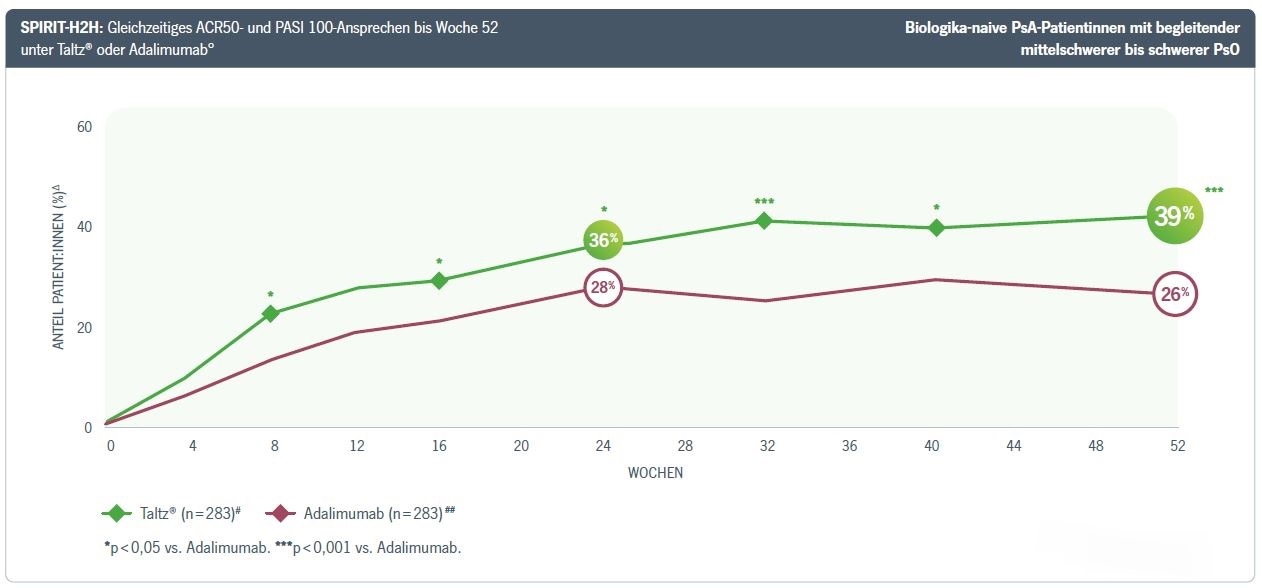
TNF-Inhibitoren (z. B. Adalimumab) können PsA-Symptome effektiver lindern als klassische DMARDs wie Methotrexat.4 Sind diese also weiterhin der Goldstandard? In der SPIRIT-H2H-Studie5 wurde die Wirksamkeit von Adalimumab mit der des IL-17A-Inhibitors Taltz® (Ixekizumab) direkt verglichen. Das Ergebnis: Taltz® war Adalimumab im gleichzeitigen Ansprechen auf Gelenk- und Hautsymptome überlegen.5 Konkret wurde der primäre kombinierte Endpunkt des gleichzeitigen Erreichens eines ACR50- und PASI 100-Ansprechens untersucht.5
Nach 24 Wochen erreichten mit Taltz® 36 % der Teilnehmenden diesen kombinierten Endpunkt versus 28 % mit Adalimumab. Somit war Taltz® dem TNFα-Blocker im primären Endpunkt überlegen. Die deutlich bessere Wirksamkeit hielt bis zu 52 Wochen an.5 (Abb. 1).
Abbildung 1: Gleichzeitiges ACR50- und PASI 100-Ansprechen bis Woche 52 unter Taltz® oder Adalimumab. Δ Berechnet mittels logistischer Regression mit Non-Responder Imputation (NRI) für fehlende Werte. # Taltz®: Patient:innen mit aktiver PsA ohne begleitende mittelschwere bis schwere Pso: Initial 2 x 80 mg, dann alle 4 Wochen 1 x 80 mg. Patient:innen mit PsA und begleitender mittelschwerer bis schwerer Pso: Initial 2 x 80 mg, dann 1 x 80 mg alle 2 Wochen in Woche 2–12; danach 1 x 80 mg alle 4 Wochen. ## Adalimumab: Bei Patient:innen mit aktiver PsA und ohne mittelschwere bis schwere Pso: Initial 1 x 40 mg, dann alle 2 Wochen 1 x 40 mg. Patient:innen mit PsA und mittelschwerer bis schwerer Pso: Initial 2 x 40 mg, dann alle 2 Wochen 1 x 40 mg ab Woche 1. ° Der primäre Endpunkt der SPIRIT-H2H-Studie war die Überlegenheit von Taltz® vs. Adalimumab in Woche 24: gemessen am Anteil der Patient:innen, die gleichzeitig ACR50 und PASI 100 erreichten.
ACR50: American College of Rheumatology, 50 % Ansprechen; H2H: Head-to-Head; NRI: Non-Responder Imputation; PASI 100: 100%ige Verbesserung der PASI-(Psoriasis Area Severity Index) Kriterien im Vergleich zum Ausgangswert; PsA: Psoriasis-Arthritis; Pso: Plaque-Psoriasis+. Modifiziert nach 5.
Eckdaten der SPIRIT-H2H-Studie:5
Frühzeitige Therapie mit Taltz® kann Progression reduzieren
Entscheidend für die Patientenzufriedenheit und den Therapieerfolg ist eine langfristige Wirksamkeit – die Betroffenen möchten ihre Lebensqualität dauerhaft zurückgewinnen.6 Dies kann gelingen, wenn das Fortschreiten der Erkrankung gestoppt wird. Denn eine Progression bedeutet nicht nur eine Zunahme der Schmerzen, sie kann zudem irreversible Gelenkschäden verursachen.
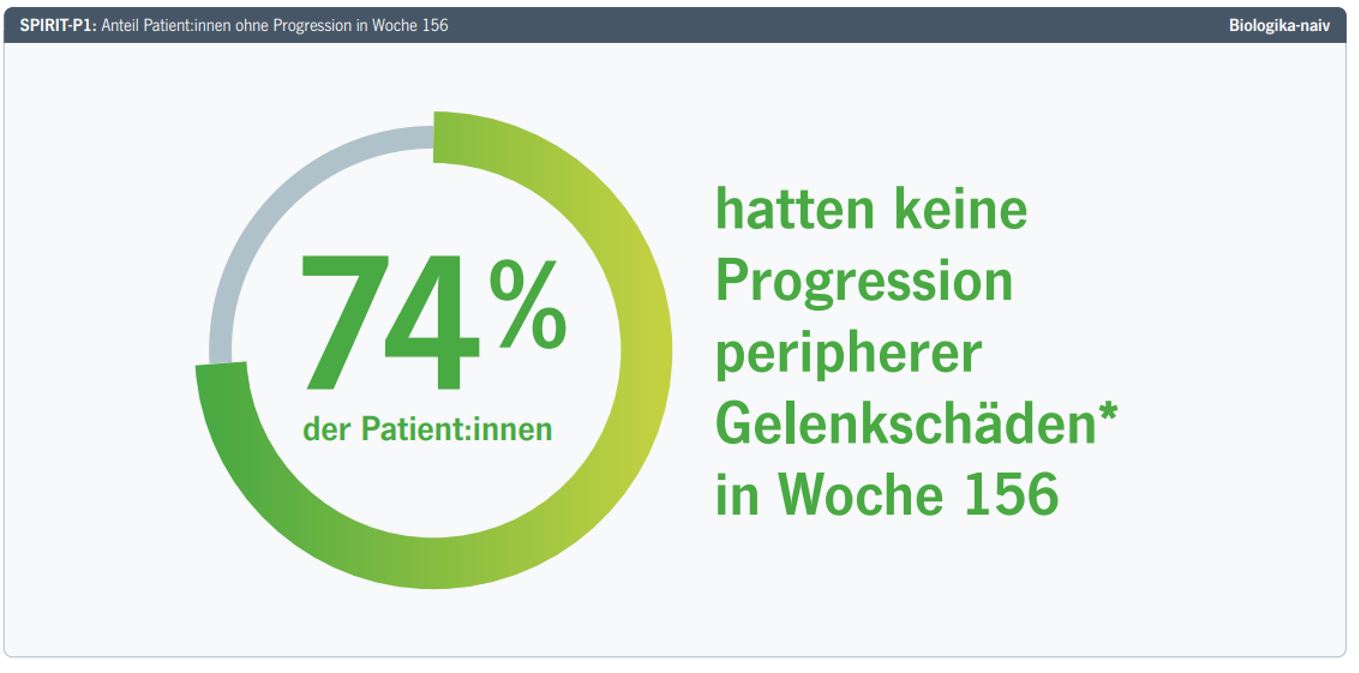
Taltz® kann die Progression von Gelenkschäden verhindern: In der SPIRIT-P1-Studie& zeigten 74 % der Patient:innen unter Taltz® keine Progression peripherer Gelenkschäden in einem Zeitraum von 3 Jahren (Abb. 2).6
Abbildung 2: Anteil der Biologika-naiven PsA-Patient:innen, die keine oder eine minimale Progression in der SPIRIT-P1-Studie aufwiesen. 74 % entsprechen 81 Patient:innen. * Definiert als mTSS-Veränderung ≤ 0,5 gegenüber Baseline bei Biologika-naiven Patient:innen. Berechnet mittels linearer Extrapolation für fehlende mTSS-Werte, wenn die Patient:innen einen Baseline- und mindestens einen post-Baseline-Wert in Woche 52, 108 oder 156 aufwiesen. mTSS: modified Total Sharp Score. Modifiziert nach 6.
Das Ergebnis zeigt: Gerade Biologika-naive PsA-Patient:innen können von einer frühzeitigen Therapie mit Taltz® profitieren.
Je früher Taltz® zur Behandlung der PsA eingesetzt wird, desto eher können die Gelenke erhalten werden bzw. eine Progression peripherer Gelenkschäden verhindert werden, insbesondere bei Biologika-naiven Patient:innen.6
Fazit:
Mit einem Medikament alle Domänen im Blick:
Taltz®
- wirkt gleichzeitig auf Gelenk und Haut5
- verbessert die Symptome schnell (bereits nach 2 Wochen)7
- wirkt anhaltend – bis zu 3 Jahre bestätigt6
- ist gut verträglich1,8
- ist einfach in Dosierung und Handhabung9
Warten Sie bei Ihrem nächsten PsA-Patienten nicht zu lange und denken Sie an Taltz® – denn Taltz® ist für heute und morgen!
Haben Sie bereits Erfahrungen mit Taltz® in der axSpA§-Therapie gesammelt? Lesen Sie hier spannende Patientenfälle:
Bringen Sie jetzt Ihre axSpA°-Patient:innen zurück ins aktive Leben – mit Taltz®!
Axiale Spondyloarthritis°: Mit Taltz® wirksam Rückenschmerzen bekämpfen
Abkürzungen
IL17-Ai: Interleukin 17-A-Inhibitor
NSAR: Nichtsteroidale Antirheumatika
DMARD: krankheitsmodifizierende Antirheumatika
TNF: Tumornekrosefaktor
bDMARD: biologisches krankheitsmodifizierendes Antirheumatikum
ACR50: American College of Rheumatology, 50 % Ansprechen;
PASI 100: 100%ige Verbesserung der PASI-(Psoriasis Area Severity Index) Kriterien im Vergleich zum Ausgangswert
Fußnoten
+ Taltz®, allein oder in Kombination mit Methotrexat, ist angezeigt für die Behandlung erwachsener Patienten mit aktiver Psoriasis-Arthritis, die unzureichend auf eine oder mehrere krankheitsmodifizierende Antirheumatika (DMARD) angesprochen oder diese nicht vertragen haben.
§ Axiale Spondyloarthritis: Ankylosierende Spondylitis (Röntgenologische axiale Spondyloarthritis): Taltz® ist angezeigt für die Behandlung erwachsener Patienten mit aktiver röntgenologischer axialer Spondyloarthritis, die auf eine konventionelle Therapie unzureichend angesprochen haben. Nicht-röntgenologische axiale Spondyloarthritis: Taltz® ist angezeigt für die Behandlung erwachsener Patienten mit aktiver nichtröntgenologischer axialer Spondyloarthritis mit objektiven Anzeichen einer Entzündung, nachgewiesen durch erhöhtes C-reaktives Protein (CRP) und/oder Magnetresonanztomographie (MRT), die unzureichend auf nicht-steroidale Antirheumatika (NSAR) angesprochen haben.
& Limitationen: This study did not have a placebo or active control group beyond week 24, was not powered to compare ixekizumab dosing regimens and was limited to bDMARD-naı¨ve patients.
Quellen
- Aktuelle Taltz® Fachinformationen
- Haugeberg G, et al. RMD Open 2020;6:e001223.
- Psoriasis-Arthritis: Symptome und Verlauf - NetDoktor.ch (zuletzt aufgerufen am 09.02.2024).
- Gossec L, et al. Ann Rheum Dis. 2020;79(6):700–12.
- Mease PJ, et al. Ann Rheum Dis 2020;76:123–131.
- Chandran V, et al. Rheumatology (Oxford). 2020;59:2774–2784.
- Mease PJ, et al. Ann Rheum Dis 2017;76:79–87.
- Deodhar A, et al. Arthritis Rheumatol. 2022;74(suppl 9) Abstract Number 1042.
- Duffin KC, et al. Med Devices (Auckl.) 2016;9:361–369.
PP-IX-DE-4094